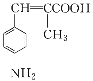
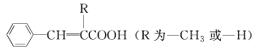题目内容
【题目】向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
选项 | 操作及现象 | 结论 |
A | 加入AgNO3溶液,生成白色沉淀,再加稀盐酸沉淀不溶解 | 原溶液中有Cl-存在 |
B | 通入Cl2后,溶液变为深黄色,继续加入淀粉溶液后溶液变蓝 | 原溶液中有I-存在 |
C | 加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解时 | 原溶液中有 |
D | 加入稀盐酸,生成的气体能使澄清石灰水变浑浊 | 原溶液中有 |
A.AB.BC.CD.D
【答案】B
【解析】
A.在加入盐酸之前生成的可能是AgCl沉淀也可能是碳酸银沉淀等等,但是后面加入盐酸后可以转化为AgCl,所以沉淀不溶解,因此,不能确定原溶液里是否有Cl-是存在,A错误;
B.氯气能将碘离子氧化为碘单质,碘水溶液为棕黄色,碘遇淀粉变蓝色,B正确;
C.硝酸根在酸性条件下有强氧化性。若溶液中含有亚硫酸根或亚硫酸,加入Ba(NO3)2溶液后,都能生成白色沉淀,加稀盐酸酸化后,亚硫酸钡能被硝酸根氧化成硫酸钡,因此,不能确定原溶液中是否有硫酸根离子存在,C错误;
D.碳酸根、碳酸氢根、亚硫酸根、亚硫酸氢根遇到盐酸,均会生成能使澄清石灰水变浑浊的气体,因此,不能确定原溶液中有碳酸根离子,D错误;
答案选B。

【题目】氮的氧化物和氮的氢化物的任意排放均会对环境造成污染,因此关于其转化的研究对于消除环境污染有着重要意义。
(1)已知T℃时,有如下反应:
反应I:4NH3(g) + 6NO(g)![]() 5N2 ( g) + 6H2O(g) △H = -1804 kJmol-1
5N2 ( g) + 6H2O(g) △H = -1804 kJmol-1
反应II:N2(g) +2O2(g) ![]() 2NO2(g) △H = +67.8 kJmol-1
2NO2(g) △H = +67.8 kJmol-1
反应III:2NO(g) + O2 (g) ![]() 2 NO2 (g) △H =-116.2 kJmol-1
2 NO2 (g) △H =-116.2 kJmol-1
试写出T℃ 时,NH3与NO2反应生成不污染环境的物质的热化学反应方程式 ______。
(2)T℃时,向2L密闭容器中加入一定量的NO2、NO和O2,发生(1)中反应III,不同时间测得各物质的部分浓度(molL-1) 如下表所示:
时间( min) | NO | O2 | NO2 |
0 | a | 0.30 | 0.10 |
10 | 0.14 | 0.27 | b |
20 | 0.10 | c | 0.20 |
30 | d | 0.24 | 0.22 |
40 | 0.08 | e | f |
①温度不变,反应达平衡后容器中的压强与最初加入气体时的压强之比为_______。
②反应的前 20 min 的平均反应速率v(NO)=________molL-1·min-1。
③若温度不变,平衡后将反应容器压缩为1L,达到新的平衡后,c(O2)_____0.48molL-1(填“>”“<”或“ =”)。
(3)某化学兴趣小组利用电解原理设计实验消除NH3 与 NO对环境的影响, 并制取KOH溶液和H2SO4溶液,其工作原理如下图所示:
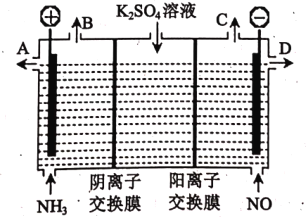
①从出口B、C产生的气体相同,该气体是_____:从出口 D 得到的溶液是____。
②电解槽左池中发生的电极反应式为________ 。
③电解一段时间,两电极共收集到22.4L气体(标准状况下)时,理论上将生成____________mol KOH。