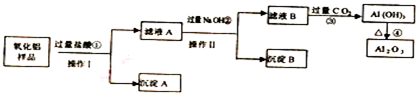
题目内容
17.氮化钠(Na3N)晶体熔融时能导电.下列描述正确的是( )| A. | 构成晶体的两种微粒电子层结构相同 | |
| B. | 构成晶体的两种微粒半径相等 | |
| C. | 构成晶体的两种微粒的核外电子能量相同 | |
| D. | 构成晶体的两种微粒的电子层数不同 |
分析 氮化钠(Na3N)晶体熔融时能导电,说明氮化钠属于离子晶体,由Na+、N3-离子构成,核外电子数均为10,电子层结构相同,核电荷数越大离子半径越小,核电荷数不同、离子半径不同,核外电子能量不同.
解答 解:A.氮化钠(Na3N)晶体熔融时能导电,说明氮化钠属于离子晶体,由Na+、N3-离子构成,核外电子数均为10,电子层结构相同,故A正确;
B.电子层结构相同,核电荷数越大离子半径越小,故离子半径:Na+<N3-,故B错误;
C.Na+、N3-离子核电荷数不同、离子半径不同,核外电子能量不同,故C错误;
D.由Na+、N3-离子构成,核外电子数均为10,电子层相同,故D错误,
故选A.
点评 本题考查结构与性质关系、晶体类型与性质及离子半径大小比较等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
5.分子式为C7H14O2的有机物A,有果香味,不能使紫色石蕊试液变红,但可在酸性条件下水解生成有机物B和C,其中B的水溶性呈酸性,C不能发生消去反应生成烯烃,但能催化氧化生成醛或酮,则A可能的结构共有( )
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 加入铝粉放出H2的溶液中:Al3+、K+、SO42-、Cl- | |
| B. | 1.0 mol•L-1的KNO3溶液中:Na+、Fe2+、Cl-、SO42- | |
| C. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液中:K+、Cu2+、SO42-、NO3- |
2.将0.5mol•L-1的Na2CO3溶液与amol•L-1的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断正确的是( )
| A. | c(Na+)>2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则可确定a>0.5 | |
| D. | 若c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c (H2CO3),则可确定a=0.5 |
9.有机物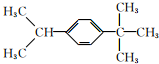 的一氯化物共有(不考虑立体异构)( )
的一氯化物共有(不考虑立体异构)( )
 的一氯化物共有(不考虑立体异构)( )
的一氯化物共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 7种 |
6.符合下列条件的有机物中,同分异构体(不考虑立体异构)数目最多的是( )
| A. | 分子式为C5H10且能使溴的CCl4溶液褪色 | |
| B. | 分子式为C7H16且含有三个甲基 | |
| C. | 分子式为C4H8O2且能与NaOH溶液反应 | |
| D. | 分子式为C4H10O且能与钠反应 |
7.在光照条件下CH4和Cl2反应,不可能生成的物质是( )
| A. | H2 | B. | HCl | C. | CH3Cl | D. | CCl4 |
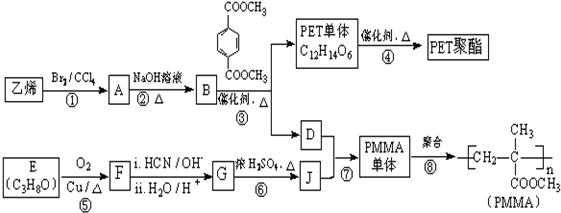
 (R、R′代表烃基,可相同也可不同)
(R、R′代表烃基,可相同也可不同)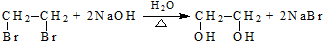 .
. .
. .
. .
. .
.