题目内容
6.铊盐与氰化钾被列为A级危险品,铊(Tl)与铝同主族,原子序数为81,Tl3+与Ag在酸性介质中发生反应:Tl3++2Ag═Tl++2Ag+且已知Ag++Fe2+═Ag+Fe3+,则下列推断正确的是( )| A. | 铊位于第五周期ⅢA族 | |
| B. | 氧化性:Tl3+>Ag+>Fe3+ | |
| C. | Tl(OH)3与Al(OH)3相似,也是两性氢氧化物 | |
| D. | Tl+最外层有3个电子 |
分析 A、根据原子序数推断元素周期表中的位置;
B、氧化还原反应中氧化剂的氧化性大于氧化产物,依据题干反应判断;
C、同主族从上到下,金属元素的最高价氧化物的水化物的碱性增强;
D、依据铊(Tl)与铝同主族,最外层电子数为3.
解答 解:A、原子序数为81,和铝同主族,结合核外电子排布规律写出原子结构示意图判断,铊位于第六周期第ⅢA族,故A错误;
B、Tl3++2Ag=Tl++2Ag+,且Ag++Fe2+=Ag+Fe3+.氧化剂Tl3+的氧化性大于氧化产物Ag+,氧化剂Ag+的氧化性大于氧化产物Fe3+,所以氧化性顺序为Tl3+>Ag+>Fe3+,故B正确;
C、同主族从上到下,金属元素的最高价氧化物的水化物的碱性增强,则Tl(OH)3的碱性大于Al(OH)3,不是两性氢氧化物,故C错误;
D、铊(Tl)与铝同主族,主族元素原子最外层电子相同,则Tl+最外层有2个电子,故D错误;
故选B.
点评 本题考查了氧化还原反应的概念应用,规律分析和判断,元素周期表中位置的推断,熟练掌握氧化还原反应的实质和强弱规律,是解题的关键.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
17.下列有关物质的用途说法不正确的是( )
| A. | 乙烯可作为部分水果或鲜花生长调节剂 | |
| B. | 乙炔燃烧时火焰温度高,氧炔焰可用于焊接或切割金属 | |
| C. | 甲醛的水溶液-福尔马林可用于杀菌、防腐 | |
| D. | 乙醇可用于萃取溴水中的溴单质 |
14.下列方法中不可以鉴别Fe3+和Fe2+的是( )
| A. | 通过物理方法观察他们颜色的区别 | |
| B. | 向两种溶液中加入NaOH溶液 | |
| C. | 向两种溶液中加入KSCN溶液 | |
| D. | 向两种溶液中加入氯水后再加入KSCN溶液 |
11.下列有关实验的描述正确的是( )
| A. | 氢氧化钠固体保存在配有玻璃塞的细口瓶中 | |
| B. | 将SO2通入品红溶液或KMnO4酸性溶液均能使它们褪色,均可证明SO2有漂白性 | |
| C. | 不能在石英坩埚中熔化氢氧化钠 | |
| D. | 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全 |
18.H、D、T、H+可以用来表示( )
| A. | 化学性质不同的氢原子 | B. | 四种不同的元素 | ||
| C. | 氢元素的四种不同粒子 | D. | 四种不同的氢元素 |
16.下列有机物或有机物组合,在现有条件下不能发生聚合反应的是( )
| A. |  和 和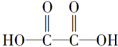 | B. | 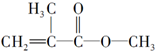 | ||
| C. |  | D. | C(CH3)4 |
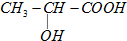 )及其盐广泛应用于食品、医药、化工等领域.有一种制备乳酸方法如下:
)及其盐广泛应用于食品、医药、化工等领域.有一种制备乳酸方法如下: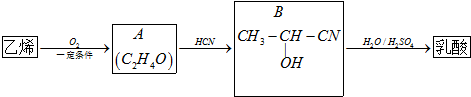
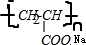 .
. 用碱性锌锰电池做电源进行电解实验,装置如图.图中A装置中盛1L2mol/LAgNO3溶液,B装置盛1L2mol/LNa2SO4溶液,C和D为润湿的淀粉KI试纸的两端.通电后电解一段时间后,润湿的淀粉KI试纸的C端变蓝色.试回答:
用碱性锌锰电池做电源进行电解实验,装置如图.图中A装置中盛1L2mol/LAgNO3溶液,B装置盛1L2mol/LNa2SO4溶液,C和D为润湿的淀粉KI试纸的两端.通电后电解一段时间后,润湿的淀粉KI试纸的C端变蓝色.试回答: