题目内容
【题目】NO2 是大气污染的主要污染物之一,硝酸盐是水体污染的污染物之一,电化学降解酸性 NO3-的原理如图所示,下列说法正确的是
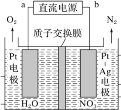
A.电源正极为 b
B.阴极电极反应式为 2NO3-+ 6H2O +10e-= N2↑+12 OH-
C.两电极上产生的气体物质的量之比 n(O2):n(N2) = 5:2
D.将阳极换成铜电极,反应不发生变化
【答案】C
【解析】
A.右边是NO3-变为N2,化合价降低得到电子,在阴极反应,因此电源负极为 b,故A错误;
B. 阴极电极反应式为 2NO3-+ 12H+ +10e-= N2↑+6 H2O,故B错误;
C. 根据得失电子守恒,5mol O2 —20mol e-—2mol N2,因此两电极上产生的气体物质的量之比 n(O2):n(N2) = 5:2,故C正确;
D. 将阳极换成铜电极,阳极是铜失去电子,故D错误。
综上所述,答案为B。

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目