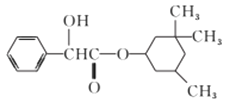
题目内容
【题目】按要求填空:
(1)质量数为37的氯原子符号为_______。
(2)S2-的结构示意图为______。
(3)氮原子的电子式为______,N2的电子式为______,NH4+的电子式为_________
(4)磷原子的核外电子排布式为______,其价电子排布式为_____, 其价电子排布图为_____。
【答案】 3717Cl(或37Cl) 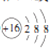
![]()
![]()
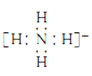 1s22s22p63s23p3{或[Ne]3s23p3} 3s23p3
1s22s22p63s23p3{或[Ne]3s23p3} 3s23p3 ![]()
【解析】(1)Cl的质子数为17,质量数为37,则质量数为37的氯原子符号为![]() 或37Cl;故答案为:
或37Cl;故答案为: ![]() 或37Cl
或37Cl
(2)硫离子最外层得到两个电子达到8电子稳定结构,所以其结构示意图为:![]() ;故答案为:
;故答案为:![]()
(3)氮原子最外层有5个电子,有一对孤对电子,氮原子的电子式为:![]() ;氮气分子的电子式为
;氮气分子的电子式为![]() ;NH4+的电子式为
;NH4+的电子式为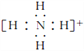 ;故答案为:
;故答案为:![]() 、
、![]() 、
、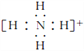
(4)磷元素核外有15个电子,根据书写规则知有3层,s轨道最多容纳两个电子,p轨道最多容纳6个电子,所以磷原子的核外电子排布式为1s22s22p63s23p3或[Ne]3s23p3;价电子为最外层的电子数,所以排布为3s23p3;价电子排布图也要顾及先向上排满,再排向下;所以排布图为:![]() 。故答案为:1s22s22p63s23p3或[Ne]3s23p3 、 3s23p3 、
。故答案为:1s22s22p63s23p3或[Ne]3s23p3 、 3s23p3 、 ![]()

【题目】科学家正在研究温室气体CH4、CO2的转化和利用。
(1)在Ni基催化剂的作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni外围价电子中有_________对成对电子。
②CH4、CO2、H2分子中有孤对电子的是_________.
(2)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数如下表。CH4与H2O形成的水合物俗称“可燃冰”。
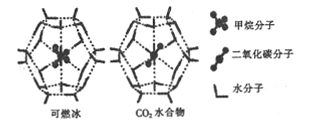
参数 分子 | 分子直径/mm | 分子与H2O的结合能(E) |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | y |
①CO2水合物分子间存在的两种作用力是___________.
②为开采深海海底的“可燃冰”,科学家已经证明可用CO2置换CH4。已知上图中笼状结构的空腔直径为xnm,根据上述图表,从物质的结构与性质的角度分析:x_____0.512;y_______16.40。(填“>”“<"或“=”)
③写出CH4的一种等电子体: __________;SiO2与CO2是否互为等电子体?_________(填“是”或“不是”),理由是________.