题目内容
为了防止或减少机动车尾气和燃煤产生的烟气对空气的污染,人们采取了很多措施。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g)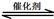 2CO2(g)+ N2(g) △H<0,
2CO2(g)+ N2(g) △H<0,
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
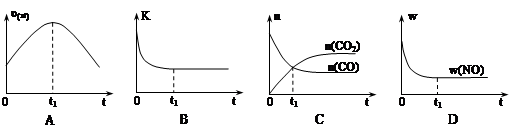
(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol ①
2NO2(g)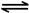 N2O4(g) ΔH=-56.9 kJ/mol ②
N2O4(g) ΔH=-56.9 kJ/mol ②
H2O(g) = H2O(l) ΔH=-44.0 kJ/mol ③
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
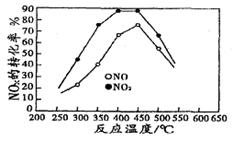
(3)用NH3催化还原NOX也可以消除氮氧化物的污染。如图,采用NH3作还原剂,烟气以一定的流速通过催化剂,通过测量逸出气体中氮氧化物含量,从而可确定烟气脱氮率,反应原理为:NO(g) +NO2(g)+2NH3(g)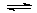 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。
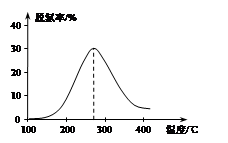
①该反应的△H 0(填“>”、“=”或 “<”)。
②对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),
则上述反应的KP= 。
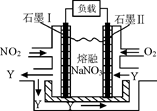
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨I为电池的 极。 该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。
(5)硝酸工业尾气中氮氧化物(NO和NO2)可用尿素〔CO(NH2)2〕溶液除去。反应生成对大气无污染的气体。1 mol尿素能吸收工业尾气中氮氧化物(假设NO、NO2体积比为1︰1)的质量为 g。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g)
 2CO2(g)+ N2(g) △H<0,
2CO2(g)+ N2(g) △H<0,若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
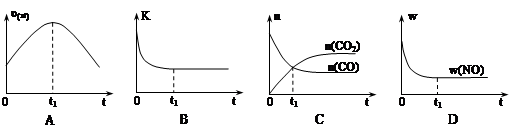
(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol ①
2NO2(g)
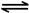 N2O4(g) ΔH=-56.9 kJ/mol ②
N2O4(g) ΔH=-56.9 kJ/mol ②H2O(g) = H2O(l) ΔH=-44.0 kJ/mol ③
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
(3)用NH3催化还原NOX也可以消除氮氧化物的污染。如图,采用NH3作还原剂,烟气以一定的流速通过催化剂,通过测量逸出气体中氮氧化物含量,从而可确定烟气脱氮率,反应原理为:NO(g) +NO2(g)+2NH3(g)
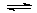 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。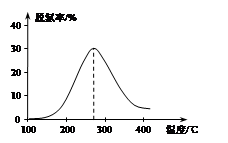
①该反应的△H 0(填“>”、“=”或 “<”)。
②对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),
则上述反应的KP= 。
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨I为电池的 极。 该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。

(5)硝酸工业尾气中氮氧化物(NO和NO2)可用尿素〔CO(NH2)2〕溶液除去。反应生成对大气无污染的气体。1 mol尿素能吸收工业尾气中氮氧化物(假设NO、NO2体积比为1︰1)的质量为 g。
(1)B D (各1分,共2分,选错不得分)
(2)CH4(g)+N2O4(g)=N2(g)+2H2O(l)+CO2(g) △H=" —898.1kJ/mol" (2分)
(3)①<(2分) ②P(N2)2P(H2O)3/P(NO)P(NO2)P(NH3)2(2分)
(4)负 (2分) NO2+NO3- -e- =N2O5 (2分)
(5)76g(2分)
(2)CH4(g)+N2O4(g)=N2(g)+2H2O(l)+CO2(g) △H=" —898.1kJ/mol" (2分)
(3)①<(2分) ②P(N2)2P(H2O)3/P(NO)P(NO2)P(NH3)2(2分)
(4)负 (2分) NO2+NO3- -e- =N2O5 (2分)
(5)76g(2分)
试题分析:(1)可逆反应达化学平衡状态时正逆反应速率不再变化,所以A错误;该物质的浓度在化学平衡时保持不变,所以K不再变化,B正确;对于恒容容器而言,各物质的物质的量不再改变,所以C错误;平衡时NO的质量分数不再改变,正确,所以答案选BD;
(2)根据盖斯定律,目标方程式=①-②+③×2,所以CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式为CH4(g)+N2O4(g)=N2(g)+2H2O(l)+CO2(g) △H= —898.1kJ/mol;
(3)据图可知,当反应达平衡后继续升温,脱氮率降低,说明升温,平衡逆向移动,所以正向是放热反应,△H<0;根据平衡常数的表达式,用平衡压强表示的平衡常数为KP=P(N2)2P(H2O)3/P(NO)P(NO2)P(NH3)2
(4)在该反应中,二氧化氮中氮元素化合价升高,发生氧化反应,负极发生氧化反应,所以石墨I为电池的的负极,该电池在使用过程中石墨I电极上生成氧化物Y,则Y是N2O5,电极反应式为NO2+NO3- -e- =N2O5;
(5)NO和NO2与尿素〔CO(NH2)2〕反应生成无污染物质是氮气、二氧化碳、水,化学方程式为
NO+NO2+CO(NH2)2=2N2+2H2O+CO2,所以1 mol尿素能吸收NO和NO2的物质的量是1mol,其质量为76g。

练习册系列答案
相关题目
 CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1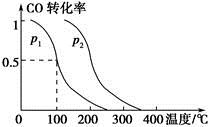
 CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是_________________________________________________
CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是_________________________________________________ 4NO(g)+CO2(g)+2H2O(g) △H1<0
4NO(g)+CO2(g)+2H2O(g) △H1<0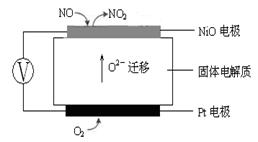
 2CO2(g)+2H2O(l) ΔH1="-870.3" kJ·mol-1
2CO2(g)+2H2O(l) ΔH1="-870.3" kJ·mol-1 H2(g)+CO2(g) ΔH2;
H2(g)+CO2(g) ΔH2;