题目内容
【题目】用适当的化学用语来表示下列反应原理
(1)氢氧化亚铁放置于空气中,颜色发生改变,有关化学方程式:;
(2)小苏打溶于水,其电离方程式:;
(3)铁红中铁的化合价为: , 它与盐酸反应的离子方程式为;
(4)明矾[KAl(SO4)212H2O]能净水是由于其溶于水后生成了(写化学式);
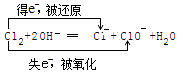
(5)工业上制取漂白液,有关离子方程式并用双线桥标明电子得失: .
【答案】
(1)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(2)NaHCO3=Na++HCO3﹣
(3)+3; Fe2O3+6H+=2Fe3++3H2O
(4)Al(OH)3(胶体)
(5)
【解析】解:(1)氢氧化亚铁在空气中会迅速变灰绿色、最后变为红褐色,氢氧化亚铁与氧气和水发生反应生成氢氧化铁,反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
所以答案是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(2)碳酸为弱酸,NaHCO3是弱酸的酸式盐,电离方程式为:NaHCO3=Na++HCO3﹣,
所以答案是:NaHCO3=Na++HCO3﹣;(3)铁红为氧化铁,化学式为Fe2O3,氧显﹣2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x×2+(﹣2)×3=0,则x=+3价,氧化铁和盐酸反应生成氯化铁和水,离子反应为:Fe2O3+6H+=2Fe3++3H20,
所以答案是:+3;Fe2O3+6H+=2Fe3++3H2O;(4)明矾[KAl(SO4)212H2O]作为净水剂是因为明矾溶于水发生水解反应,生成氢氧化铝胶体,氢氧化铝胶体可以吸附杂质,反应的离子方程式为:Al3++3H2O=Al(OH)3(胶体)+3H+;
所以答案是:Al(OH)3(胶体);(5)工业上制取漂白液,Cl2+2NaOH═NaCl+NaClO+H2O中,只有Cl元素的化合价变化,Cl元素的化合价由0升高为+1价,由0降低为﹣1价,该反应中Cl既被氧化也被还原,该反应中转移电子为e﹣,则双线桥标得失电子数方法为 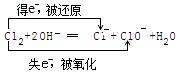 ;
;
所以答案是:  .
.

 名校通行证有效作业系列答案
名校通行证有效作业系列答案