题目内容
(4分)硝酸铜受热易分解:2Cu(NO3)2 2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO
2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO  2Cu2O+ O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2
2Cu2O+ O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2 N2O4,2NO2=2NO+O2等反应)。
N2O4,2NO2=2NO+O2等反应)。
现取5.64gCu(NO3)2无水晶体,在一定温度下使其分解,将生成的气体及时导出并用足量的NaOH溶液充分吸收。
⑴若该质量的无水硝酸铜经加热完全分解,其中的铜元素全部转化为氧化铜,则氧化铜的质量是__________g。
⑵若该质量的无水硝酸铜完全分解,铜元素全部转化为氧化亚铜,反应过程中生成的气体被足量的NaOH溶液充分吸收后,还有多余的气体,则多余的气体是________(填分子式),其体积(标准状况)是_____________L。
⑶若该质量的无水硝酸铜分解后的残留固体中含有1.60g CuO,则残留固体的质量可能
是_________g。
 2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO
2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO  2Cu2O+ O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2
2Cu2O+ O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2 N2O4,2NO2=2NO+O2等反应)。
N2O4,2NO2=2NO+O2等反应)。现取5.64gCu(NO3)2无水晶体,在一定温度下使其分解,将生成的气体及时导出并用足量的NaOH溶液充分吸收。
⑴若该质量的无水硝酸铜经加热完全分解,其中的铜元素全部转化为氧化铜,则氧化铜的质量是__________g。
⑵若该质量的无水硝酸铜完全分解,铜元素全部转化为氧化亚铜,反应过程中生成的气体被足量的NaOH溶液充分吸收后,还有多余的气体,则多余的气体是________(填分子式),其体积(标准状况)是_____________L。
⑶若该质量的无水硝酸铜分解后的残留固体中含有1.60g CuO,则残留固体的质量可能
是_________g。
(1)2.4g(1分);⑵O2,0.168L(各1分,共2分);⑶3.48g或2.32g(共1分);
(1)5.64gCu(NO3)2的物质的量是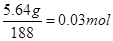 ,所以可以生成0.03mol氧化铜,质量是0.03mol×80g/mol=2.4g。
,所以可以生成0.03mol氧化铜,质量是0.03mol×80g/mol=2.4g。
(2)如果生成氧化亚铜,则方程式为4Cu(NO3)2 2Cu2O+8NO2↑+3O2↑.生成的气体溶于水发生反应的方程式为4NO2+O2+2H2O=4HNO3,所以氧气是过量的。0.03mol硝酸铜生成0.06molNO2和0.0225mol氧气,所以通入水后剩余氧气是0.0225mol-0.015mol=0.0075mol,标准状况下的体积是0.168L。
2Cu2O+8NO2↑+3O2↑.生成的气体溶于水发生反应的方程式为4NO2+O2+2H2O=4HNO3,所以氧气是过量的。0.03mol硝酸铜生成0.06molNO2和0.0225mol氧气,所以通入水后剩余氧气是0.0225mol-0.015mol=0.0075mol,标准状况下的体积是0.168L。
(3)1.60g CuO是0.02mol。如果残留物是氧化铜和氧化亚铜构成的,则氧化亚铜的质量是0.005mol×144g/mol=0.72g,则总质量是2.32g;如果是氧化铜和硝酸铜构成的,则硝酸铜是0.01mol,质量是1.88g,则总质量是3.48g。
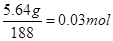 ,所以可以生成0.03mol氧化铜,质量是0.03mol×80g/mol=2.4g。
,所以可以生成0.03mol氧化铜,质量是0.03mol×80g/mol=2.4g。(2)如果生成氧化亚铜,则方程式为4Cu(NO3)2
 2Cu2O+8NO2↑+3O2↑.生成的气体溶于水发生反应的方程式为4NO2+O2+2H2O=4HNO3,所以氧气是过量的。0.03mol硝酸铜生成0.06molNO2和0.0225mol氧气,所以通入水后剩余氧气是0.0225mol-0.015mol=0.0075mol,标准状况下的体积是0.168L。
2Cu2O+8NO2↑+3O2↑.生成的气体溶于水发生反应的方程式为4NO2+O2+2H2O=4HNO3,所以氧气是过量的。0.03mol硝酸铜生成0.06molNO2和0.0225mol氧气,所以通入水后剩余氧气是0.0225mol-0.015mol=0.0075mol,标准状况下的体积是0.168L。(3)1.60g CuO是0.02mol。如果残留物是氧化铜和氧化亚铜构成的,则氧化亚铜的质量是0.005mol×144g/mol=0.72g,则总质量是2.32g;如果是氧化铜和硝酸铜构成的,则硝酸铜是0.01mol,质量是1.88g,则总质量是3.48g。

练习册系列答案
相关题目


