题目内容
实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:?
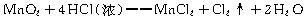
若产生的氯气的物质的量为0.5 mol。试计算:?
(1)参加反应的MnO2的质量。?
(2)参加反应的HCl的物质的量。?
(3)反应中被氧化的HCl的物质的量。
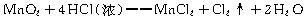
若产生的氯气的物质的量为0.5 mol。试计算:?
(1)参加反应的MnO2的质量。?
(2)参加反应的HCl的物质的量。?
(3)反应中被氧化的HCl的物质的量。
(1)43.5 g (2)2 mol (3)1 mol
根据反应的方程式可得?
MnO2+4HCl(浓)====MnCl2+Cl2↑+2H2O 被氧化的HCl的物质的量
87 g 4 mol 1 mol 2 mol
(43.5 g) (2 mol) 0.5 mol (1 mol)
MnO2+4HCl(浓)====MnCl2+Cl2↑+2H2O 被氧化的HCl的物质的量
87 g 4 mol 1 mol 2 mol
(43.5 g) (2 mol) 0.5 mol (1 mol)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
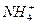 中含有的电子数为NA
中含有的电子数为NA