题目内容
8.下列物质中,既可与盐酸反应,又可与氢氧化钠溶液反应的是( )| A. | NaHSO4 | B. | NaHCO3 | C. | Al(OH)3 | D. | Na2SO3 |
分析 既能与盐酸反应又能与氢氧化钠溶液反应的物质有:两性化合物(如Al2O3、Al(OH)3等)、弱酸的铵盐(如(NH4)2CO3等)、弱酸的酸式盐(NaHCO3、NaHS等)、单质(如Al)、氨基酸等.
解答 解:A.硫酸氢钠与盐酸不反应,故A错误;
B.碳酸氢钠为弱酸的酸式盐,与盐酸、氢氧化钠都反应,故B正确;
C.氢氧化铝为两性物质,与盐酸、氢氧化钠都反应,故C正确;
D.亚硫酸钠与氢氧化钠不反应,故D错误;
故选:BC.
点评 本题考查了能和强酸、强碱反应的物质,明确物质的性质是解本题关键,注意归纳总结中学常见的既能与酸反应又能与碱反应的物质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,48g O3含有的氧原子数为NA | |
| B. | 22g CO2所含的分子数为0.5NA | |
| C. | 11.5L CO2所含的分子数为0.5NA | |
| D. | 常温常压下,NA个Cl2分子所占有的体积为22.4L |
16.下列有关化学用语表达不正确的是( )
| A. | 氮气的电子式: | |
| B. | 中子数是8的碳原子的符号:${\;}_{6}^{14}$C | |
| C. | Na的原子结构示意图: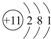 | |
| D. | 钙离子的电子式:Ca2+ |
13.下列过程中,△H<0的是( )
| A. | K(g)═K+(g)+e- | B. | Cl(g)+e-═Cl(g) | C. | KCl(s)═K++Cl-(g) | D. | Cl2(g)═2Cl(g) |
20.某溶液中加入过量的氢氧化钠溶液或过量的氨水均能生成白色沉淀,该溶液中所含的阳离子可能是( )
| A. | Na+ | B. | Mg2+ | C. | Al3+ | D. | Fe3+ |
18.对于反应:CaCO3+2HCl═CaCl2+H2O+CO2↑,下列说法正确的是( )
| A. | 用HCl和CaCl2的单位时间内浓度变化表示反应速率不同,表示的意义也不相同 | |
| B. | 可用单位时间内CaCl2浓度的变化量表示其反应速率 | |
| C. | 用CaCO3和CO2表示的化学反应速率相同 | |
| D. | 可用CaCO3浓度变化来表示反应速率,也可用水来表示反应速率 |