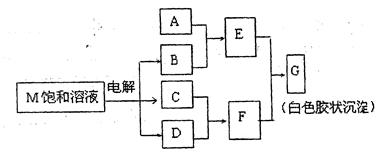
题目内容
下列有关物质结构的说法正确的是:
| A.共价化合物中各原子最外层都一定满足8电子结构 |
| B.BaO2晶体中阳离子与阴离子数目之比为1∶2 |
| C.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| D.在反应2Na2O2+2H2O ="=" 4NaOH+O2↑,既有离子键、极性键和非极性键的断裂,又有离子键、极性键和非极性键的形成 |
D
共价化合物H2O、BeCl2中H和Be两原子最外层均不是8电子结构,选项A错;BaO2晶体中阳离子是Ba2+,阴离子是O2-2,两者的物质的量之比为1∶1,选项B错;选项C中水非常稳定的原因是氢氧键键能比较大, 故选D。

练习册系列答案
相关题目
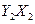 分子中Y原子轨道的杂化类型为 ,1mol
分子中Y原子轨道的杂化类型为 ,1mol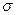 键的数目为 。
键的数目为 。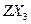 的沸点比化合物
的沸点比化合物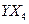 的高,其主要原因是
的高,其主要原因是  。
。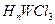 ,反应的化学方程式为 。
,反应的化学方程式为 。
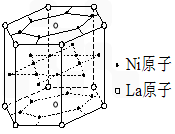
 ⅢA
ⅢA 价氧化物的水化物中,酸性最强的化合物的分子式是 ,碱性最强的化合物的化学式是 。
价氧化物的水化物中,酸性最强的化合物的分子式是 ,碱性最强的化合物的化学式是 。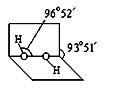
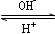 R(OH)3
R(OH)3  C.非极性键 D.配位键
C.非极性键 D.配位键