题目内容
由已知电离常数判断,下列关于SO2与Na2CO3(aq)反应的离子方程式的书写中,不合理的是
| 酸 | 电离常数 |
| 碳酸 | K1=4×10-7 K2=5.6×10-11 |
| 亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
B.SO2+H2O+CO32-=H2CO3+SO32-
C.2SO2+2H2O+CO32-=H2CO3+2 HSO3-
D.SO2+H2O+CO32-= HCO3-+HSO3-
B
解析试题分析:弱酸的电离平衡常数越大,酸性越强。根据电离平衡常数可知,酸性强弱顺序是H2SO3>HC2O3>HSO3->HCO3-,所以根据较强的酸制备减弱的酸可知,A、C、D均是正确的,B不正确,即HSO3-不能制备碳酸,答案选B。
考点:考查电离平衡常数的应用、酸性强弱比较

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
某温度时,AgCl(s)  Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是
| A.加入AgNO3,可以使溶液由c点变到d点 |
| B.加入少量水,平衡右移,Cl-浓度减小 |
| C.d点没有AgCl沉淀生成 |
| D.c点对应的Ksp等于a点对应的Ksp |
已知Ksp(AgCl)=1.8×10—10mol2?L—2,Ksp(AgI)=1.0×10—16mo2?L—2。下列说法错误的是
| A.AgCl不溶于水,不能转化为AgI |
| B.在含浓度均为0.001mol?L—1的Cl—、I—的溶液中缓慢滴AgNO3稀溶液,先析出AgI |
| C.AgI比AgCl更难溶于水,所以AgCl可转化为AgI |
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于 ×10—11mol?L—1 ×10—11mol?L—1 |
下列说法正确的是
| A.直接加热蒸干FeCl3溶液,可得FeCl3固体 |
| B.加入催化剂可加快反应速率,并提高反应物的转化率 |
| C.pH值相同的CH3COOH溶液和NH4Cl溶液中,水的电离程度相同 |
| D.可用Na2CO3溶液处理水垢中的CaSO4,转化为易于除去的CaCO3 |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | 1.77×l0–5 | 4.9×l0–10 | Ki1=4.3×l0–7 Ki2=5.6×l0–11 |
下列选项错误的是
A.等物质的量浓度的各溶液pH关系为:PH(NaCN)>PH(Na2CO3)>PH(NaHCO3)>PH(HCOONa)
B.2CN– +H2O + CO2 →HCN + CO32–
C.等物质的量浓度的HCN溶液与NaOH溶液等体积混合后溶液中:c(OH–)>c(H+),c(Na+)>c(CN–)
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–)
0.1mol/L的K2S溶液中,有关粒子的浓度大小关系正确的是
| A.c(K+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| B.c(K+)+ c(S2-) = 0.3mol/L |
| C.c(K+)=c(S2-)+c(HS-)+c(H2S) |
| D.c(OH-)=c(H+)+c(HS-)+2c(H2S) |
常温下,向20.00mL 0.1000 mol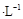 (NH4)2 SO4溶液中逐滴加入0.2000 mol
(NH4)2 SO4溶液中逐滴加入0.2000 mol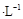 NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
下列说法正确的是
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42)>c(NH3·H2O )>c(OH-)>c(NH4+) |
一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断一定正确的是
| A.c(A-)≧c(M+) |
| B.c(A-)= c(M+) |
| C.若MA不水解,则c(OH-)<c(H+) |
| D.若MA水解,则c(OH-)>c(H+) |
