题目内容
已知某KOH样品中含水7.62%,含K2CO3 2.23%,含KOH 90%。现将1.00g 样品加入46.00mL 1.00mol/L的盐酸中,过量的酸用1.070mol/L KOH溶液中和。蒸发溶液,蒸发到无水时,可得的固体的质量
| A.3.00g | B.3.43g | C.4.50g | D.无法计算 |
B
根据反应的原理可知,最终溶质是氯化钾。根据原子守恒可知,氯化钾的物质的量是0.046L×1.00mol/L=0.046mol,固体的质量是0.046mol×74.5g/mol=3.43g,答案选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
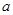 LHCl气体溶于1L水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是( )
LHCl气体溶于1L水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是( )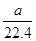 mo1·L-1
mo1·L-1 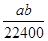 mol·L-1
mol·L-1 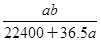 mol·L-1
mol·L-1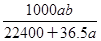 mol·L
mol·L 为阿伏加德罗常数的值,下列叙述正确的是( )
为阿伏加德罗常数的值,下列叙述正确的是( ) ·
·
 氟化氢中含有氟原子的数目为
氟化氢中含有氟原子的数目为

