题目内容
相对分子质量为100的烃完全燃烧后,生成CO2和H2O的物质的量之比以及分子结构中有四个甲基的同分异构体的数目分别是( )
| A、6:7和2 |
| B、6:7和3 |
| C、7:8和3 |
| D、7:8和4 |
考点:同分异构现象和同分异构体
专题:同系物和同分异构体
分析:先根据相对分子质量为100的烃,其分子中C原子最大数目=
=8…4,由碳原子与H原子关系可知,7个C原子饱和最多需要16个H原子,故该烃7个C原子,分子式为C7H16,结合原子守恒计算完全燃烧生成CO2和H2O的物质的量之比;该分子结构中有四个甲基,说明取代基有2个,可能是2个甲基或1个甲基和1个乙基,然后根据位置不同确定同分异构体;
| 100 |
| 12 |
解答:
解:相对分子质量为100的烃,其分子中C原子最大数目=
=8…4,由碳原子与H原子关系可知,7个C原子饱和最多需要16个H原子,故该烃7个C原子,分子式为C7H16,由原子守恒可知,1mol该烃完全燃烧生成7molCO2、8molH2O,故燃烧后生成CO2和H2O的物质的量之比为7:8,
该分子结构中有四个甲基,取代基为2个甲基,说明主链有5个碳原子,有4种结构: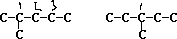 ,
,
取代基为1个甲基和1个乙基,说明主链有4个碳原子,乙基至少在3号位上,无此结构,故同分异构体的数目四4种,故选D.
| 100 |
| 12 |
该分子结构中有四个甲基,取代基为2个甲基,说明主链有5个碳原子,有4种结构:
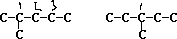 ,
,取代基为1个甲基和1个乙基,说明主链有4个碳原子,乙基至少在3号位上,无此结构,故同分异构体的数目四4种,故选D.
点评:本题考查烃的分子式确定、燃烧计算,同分异构体的确定,难度中等,确定分子式为关键,注意掌握利用商余法确定烃的分子式.

练习册系列答案
相关题目
下列金属材料中,最适合制造飞机外壳的是( )
| A、镁铝合金 | B、铜合金 |
| C、碳素钢 | D、钠钾合金 |
一定条件下存在反应:A(g)+B(g)?C(g)+D(g)△H<0.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol A和1mol B,在Ⅱ中充入1mol C和1mol D,在Ⅲ中充入2mol A和2mol B,500℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中A的物质的量比容器Ⅱ中的多 |
| D、容器Ⅰ中A的转化率与容器Ⅱ中C的转化率之和小于1 |
下列离子方程式正确的是( )
| A、氢硫酸与CuSO4溶液混合:S2-+Cu2+═CuS↓ | ||||
| B、磷酸二氢钙溶液跟足量NaOH溶液反应:3Ca2++2H2PO4-+4OH-═Ca3(PO4)2↓+4H2O | ||||
| C、硝酸亚铁溶液中滴入稀硫酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O | ||||
D、电解MgCl2溶液:2H2O+2Cl-
|
下列说法正确的是( )
| A、原子晶体中只存在非极性共价键 |
| B、稀有气体形成的晶体属于分子晶体 |
| C、干冰升华时,分子内共价键会发生断裂 |
| D、金属元素和非金属元素形成的化合物一定是离子化合物 |
由日本和中国科学家相继发现的新的高温超导材料--铁基超导材料:其成分是氟、镧(La)、氧、铁、砷(As)化合物.下列有关该材料的判断正确的是( )
| A、在周期表中,该材料所含五种元素有两种位于主族 |
| B、该超导材料所含五种元素有两种金属元素,三种非金属元素 |
| C、该超导体材料耐酸腐蚀 |
| D、在周期表中,铁属主族元素 |
关于钠及其化合物性质的叙述,正确的是( )
| A、相同条件下,在水中碳酸钠的溶解度小于碳酸氢钠的溶解度 |
| B、氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 |
| C、碳酸钠固体中混有少量碳酸氢钠,可用加热的方法除去 |
| D、质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,后者产生气体少 |