题目内容
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是
| | X | Y | |
| W | | | Z |
| T | | | |
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Y和氢三种元素形成的化合物中只有共价键
C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
D。
解析试题分析:短中期W、X、Y、Z分别是Si、N、O、Cl,T是Ge。A.X、Y、Z三种元素最低价氢化物的沸点依次升高,HCl最低,它的分子间不形成氢键;B.由X、Y和氢三种元素形成的化合物NH4NO2中含有离子键和共价键;C.物质WZ4(GeCl4)是分子晶体,熔点低、硬度小。
考点:元素周期表的位置与物质的性质推断。

练习册系列答案
相关题目
元素周期表中某区域的一些元素多用于制造半导体材料,它们是
| A.左、下方区域的金属元素 | B.金属元素和非金属元素分界线附近的元素 |
| C.右、上方区域的非金属元素 | D.稀有气体元素 |
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是
| A.W的原子序数可能是Y的原子序数的2倍 |
| B.Z元素的原子半径可能比Y元素的小 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.若Z的最高正价为+m,则X的最高正价也一定为+m |
已知钡的金属活动性处于钾和钠之间。则下列变化中可能实现的是
| A.钡可从氯化钠溶液中置换出金属钠 |
| B.钡可从冷水中置换出氢气 |
| C.钡可从硫酸铜溶液中置换出铜 |
| D.在溶液中Ba2+可氧化金属锌,生成Zn2+ |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是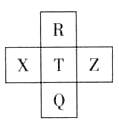
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列判断正确的是( )
| A.金属性:甲>乙>丁 |
| B.原子半径:辛>己>戊 |
| C.丙和庚的原子核外电子数相差13 |
| D.乙的单质在空气中燃烧生成只含离子键的化合物 |
氯元素的相对原子质量为35.5,氯只有35Cl和37Cl两种稳定同位素,在氯气中35Cl和37Cl的原子个数比为3∶1,则相对分子质量为70,72,74的氯气分子数之比可能是( )
| A.5∶3∶2 | B.5∶2∶2 | C.5∶2∶1 | D.9∶3∶1 |
下图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是
| R | | |
| X | Y | Z |
A.R的气态氢化物与它的含氧酸之间能发生化学反应
B.原子半径大小顺序是:Z>Y>X
C.Y、Z的单质在一定条件下均能与Fe反应
D.X、Y、Z中Z的氧化物对应的水化物的酸性最强