题目内容
19.下列有关钠的叙述,正确的是( )①钠在空气中燃烧生成氧化钠
②金属钠有强还原性
③钠与硫酸铜溶液反应,可以置换出铜
④金属钠可以保存在煤油中
⑤钠原子的最外层上只有一个电子,所以在化合物中钠的化合价显+1价.
| A. | ①②④ | B. | ②③⑤ | C. | ①④⑤ | D. | ②④⑤ |
分析 钠性质活泼,燃烧生成过氧化钠,易与空气中的水、氧气反应,在自然界中以化合态存在,与煤油不反应,且密度比煤油大,可保存在煤油中,以此解答该题.
解答 解:①钠在空气中燃烧生成过氧化钠,不加热生成氧化钠,故错误;
②金属钠原子半径较大,最外层有1个电子,易失去电子,有强还原性,故正确;
③钠与水剧烈反应,投入硫酸铜溶液中反应生成氢气和氢氧化铜,故错误;
④与煤油不反应,且密度比煤油大,可保存在煤油中,故正确;
⑤元素最高化合价与价电子有关,钠原子的最外层上只有一个电子,所以在化合物中钠的化合价显+1价,故正确.
故选D.
点评 本题考查钠的性质,题目难度不大,注意钠与硫酸铜溶液反应的性质,学习中注意相关知识的积累.

练习册系列答案
相关题目
9.当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
| A. | 当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 | |
| B. | 原电池的正极反应式为:O2十2H2O十4e-═4OH- | |
| C. | 电解后c(Na2CO3)不变,且溶液中有晶体析出 | |
| D. | 电池中c(KOH)不变;电解池中溶液pH变大 |
10.2022年北京-张家口第24届冬季奥林匹克运动会三大理念是“以运动员为中心、可持续发展、节俭办”,为了可持续发展,下列环保建议中,你认为不能采纳的是( )
| A. | 用天然气代替汽油和柴油作发动燃料 | |
| B. | 开发、使用新能源 | |
| C. | 禁止未经处理的工业废水和生活污水的任意排放 | |
| D. | 大量使用农药,提高粮食产量 |
14.一定质量的镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.下列关于反应的说法错误的是( )

| A. | 镁和铝的物质的量之比为3:2 | B. | 镁和铝转移电子数之比为1:1 | ||
| C. | 镁和铝的摩尔质量之比为8:9 | D. | 镁和铝反应所用时间之比为3:2 |
2.相同温度下,在体积相等的三个密闭容器甲、乙、丙中发生可逆反应:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
其中甲为恒温恒容容器,乙为恒温恒压容器、丙为恒容绝热容器;实验测得起始、平衡时的有关数据如下表:
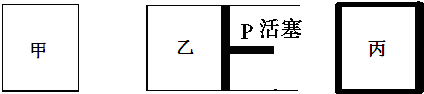
下列叙述正确的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
其中甲为恒温恒容容器,乙为恒温恒压容器、丙为恒容绝热容器;实验测得起始、平衡时的有关数据如下表:

| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 1 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A. | N2的转化率:丙是甲的二倍 | |
| B. | 三个容器内反应的平衡常数:甲=乙>丙 | |
| C. | 达平衡时氨气的体积分数:甲>乙>丙 | |
| D. | 放出热量关系:b<a<92.4 |






 .
.