题目内容
【题目】下列实验中,能证明苯酚的酸性极弱的是 ( )
A. 苯酚的水溶液中加入氢氧化钠溶液,生成苯酚钠
B. 苯酚在空气中容易被氧化为粉红色
C. 苯酚钠溶液中通入二氧化碳后,溶液由澄清变浑浊
D. 浑浊的苯酚溶液加热变澄清
【答案】C
【解析】
A、苯酚的水溶液中加入NaOH溶液,生成苯酚钠,体现苯酚的酸性,无法说明苯酚酸性极弱,故A不符合题意;
B、苯酚在空气中容易被氧化为粉红色,说明苯酚具有还原性,故B不符合题意;
C、苯酚钠溶液中通入CO2后,产生苯酚,利用相对较强酸制相对较弱酸,碳酸为弱酸,即苯酚的酸性比碳酸弱,故C符合题意;
D、升高温度,增加苯酚溶解度,与苯酚的酸性无关,故D不符合题意。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】为解决能源短缺问题,工业生产中应合理利用化学能。
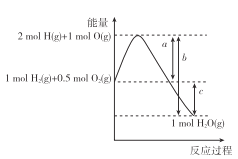
(1)25 ℃,1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为______________________。

(2)上图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从________处通入(填“a”或“b”),电池内部H+向_______(填“左”或“右”)移动。写出电池负极的电极反应式________。正极的电极反应式_______________________。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
化学键 | H—H | N—H | N≡N |
键能/kJ·mol-1 | 436 | a | 945 |
已知:N2(g)+3H2(g)===2NH3(g) ΔH=-93 kJ·mol-1。
试根据表中所列键能数据计算a的数值________。
当可逆反应中净生成N—H物质的量为2mol 时,反应放热_____________。
(4)已知:C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g)的ΔH=________。