题目内容
【题目】镍是银白色金属,具有磁性。图1为一种含镍配合物及其配体。
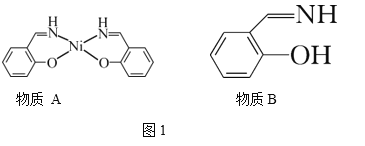
(1)Ni2+基态核外电子排布式为__________________。
(2)物质A中碳原子采取的杂化类型为__________,所含有的非金属元素的第一电离能 由小到大顺序为__________(用元素符号表示)。
(3)1 mol物质B中所含σ键的物质的量为__________mol。
(4)物质B在一定条件下水解生成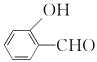 的沸点为197 ℃,而
的沸点为197 ℃,而![]() 的沸点为247 ℃,导致两种物质沸点相差较大的原因是____________。
的沸点为247 ℃,导致两种物质沸点相差较大的原因是____________。
(5)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如图2所示,则每个 Ni原子周围与之紧邻的As原子数为__________。
 。
。
【答案】1s22s22p63s23p63d8或[Ar]3d8 sp2 C<O<N 16 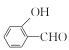 形成分子内氢键,
形成分子内氢键,![]() 形成分子间氢键,故前者沸点低于后者 6
形成分子间氢键,故前者沸点低于后者 6
【解析】
(1)镍是28号元素,Ni2+核外有26个电子,根据构造原理写电子排布式。
(2)苯环碳原子有3个![]() 键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个
键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个![]() 键,没有孤电子对,故也采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律排序。
键,没有孤电子对,故也采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律排序。
(3)单键是σ键,双键中只有1个σ键,苯环上相邻的两个碳原子间只有1个σ键,据此分析。
(4) ![]() 分子中O-H与-CHO之间形成分子内氢键,而
分子中O-H与-CHO之间形成分子内氢键,而![]() 中O-H与-CHO距离较远,只能形成分子间氢键,从氢键角度分析沸点差异。
中O-H与-CHO距离较远,只能形成分子间氢键,从氢键角度分析沸点差异。
(5)以顶点为中心,结合晶体图像分析即可。
(1)镍是28号元素,Ni2+核外有26个电子,根据构造原理可得Ni2+基态核外电子排布式为1s22s22p63s23p63d8或[Ar]3d8。
(2)苯环碳原子有3个![]() 键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个
键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个![]() 键,没有孤电子对,故也采取sp2杂化,所以物质A中碳原子都采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律可知,第一电离能由小到大顺序为C<O<N(H不参与比较)。
键,没有孤电子对,故也采取sp2杂化,所以物质A中碳原子都采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律可知,第一电离能由小到大顺序为C<O<N(H不参与比较)。
(3)单键是σ键,双键中只有1个σ键,苯环上相邻的两个碳原子间只有1个σ键。物质B中单键数有5个C-H,1个N-H,1个O-H,侧链1个C-C,1个C-O;含双键数为1个C=N;苯环共有6个σ键,所以1mol物质B中所含σ键的物质的量为16mol。
(4) ![]() 分子中O-H与-CHO之间形成分子内氢键,而
分子中O-H与-CHO之间形成分子内氢键,而![]() 中O-H与-CHO距离较远,只能形成分子间氢键,所以
中O-H与-CHO距离较远,只能形成分子间氢键,所以![]() 沸点低于
沸点低于![]() 的沸点。
的沸点。
(5)以顶点为中心,结合晶体图像分析可知,晶体中每个Ni原子周围与之紧邻的As原子数为6。