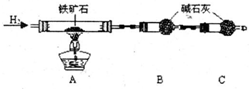
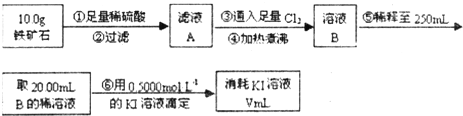
题目内容
某铁的氧化物,用7 mol•L-1的盐酸100 mL在一定条件下恰好完全溶解,所得溶液再通入0.56 L(标准状况下)的氯气时,刚好使溶液中Fe2+完全转化为Fe3+。则该氧化物的化学式可表示为( )
A. FeO B. Fe3O4 C. Fe4O5 D.Fe5O7
答案:D
提示:
提示:
n(Cl2)=0.025 mol,n(Fe2+)=0.05 mol n(Cl-)总=0.7 mol+0.05 mol=0.75 mol n(Fe3+)总=0.25 mol n(Fe3+)= n(Fe3+)总-n(Fe2+)=0.2 mol n(Fe2+): n(Fe3+)=0.05:0.2=1:4 故Fe的平均化合价为+
|

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目