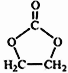
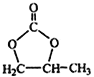
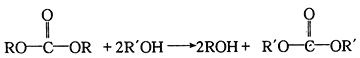题目内容
【题目】在2 L密闭容器中进行反应C(s)+H2O(g)![]() CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
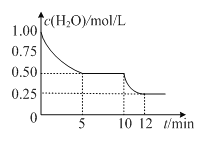
A.5 min时该反应的K值一定小于12 min时的K值
B.0~5 min内,v(H2)=0.05 mol/(L·min)
C.10 min时,改变的外界条件可能是减小压强
D.该反应混合气体的平均相对分子质量:5 min时小于12 min 时的
【答案】A
【解析】本题考查化学平衡建立的过程、影响化学平衡的因素。A.由图可知,10 min时H2O的浓度继续减小,反应向正反应方向移动,该反应正反应是吸热反应,所以10 min时改变的条件是升高温度。则5 min时该反应的K值一定小于12 min时的K值,正确;B.根据图可知,前5 min内H2O的浓度由1.00 mol/L减小为0.50 mol/L,根据v=△c/△t=(1 mol/L0.5 mol/L)/5 min=0.1 mol/(L·min),由化学计量数之比等于反应速率之比,则v(H2)=0.1 mol/(L·min),错误;C.依据题意可知该反应在2 L固定容积的容器中进行,所以不可能减小压强。且由图可知,10 min时H2O的浓度继续减小,反应向正反应方向移动,该反应正反应是吸热反应,所以是升高温度,错误;由方程式可知,该反应方程式前气体的平均相对分子质量为18、方程式后气体的平均相对分子质量为15。且12 min时平衡与5 min相比平衡正向移动了,所以该反应混合气体的平均相对分子质量:5 min时大于12 min 时的,错误;故选A。

练习册系列答案
相关题目