题目内容
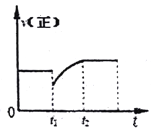
【题目】某密闭容器中的反应:3H2(g)+N2(g)![]() 2NH3(g)△H<0,其正反应速率随时间变化的情况如图所示,判断下列有关t1时刻条件变化的说法可能正确的是
2NH3(g)△H<0,其正反应速率随时间变化的情况如图所示,判断下列有关t1时刻条件变化的说法可能正确的是
A. 增大NH3浓度的同时减小N2浓度 B. 增大N2和H2的浓度
C. 扩大容器的体积 D. 降低反应温度
【答案】A
【解析】试题分析:A项增大NH3浓度的同时减小N2浓度瞬间会使逆反应速率增大,正反应速率减小,反应逆向移动,正反应速率逐渐增大达到平衡,新平衡下的正反应速率比原平衡大,故A项正确;B项增大N2和H2的浓度会瞬间增大正反应速率,逆反应速率不变,反应正向移动,正反应速率逐渐减小达到平衡,故B项错误;C项扩大容器的体积会使单位体积内该体系的分子总数减小,正逆反应速率同时减小,平衡应向使单位体积内分子数增多的方向移动,故平衡逆向移动,使正反应速率逐渐增大达到平衡,但新平衡下的正反应速率比原平衡小,故C项错误;D项该反应正向△H<0为放热反应,故降低温度正逆反应速率均减小,平衡正向移动,故正反应速率逐渐减小达到平衡,故D项错误;本题选A。

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目