题目内容
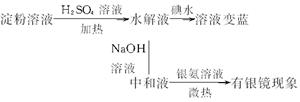
Ⅰ.某学生设计了三个实验方案,都认为可以检验淀粉的水解情况:(1)方案甲:
淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 溶液变蓝
溶液变蓝
结论:淀粉没有水解。
(2)方案乙:
淀粉液![]() 水解液
水解液![]() 无红色沉淀
无红色沉淀
结论:淀粉完全没有水解。
(3)方案丙:
淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 有红色沉淀
有红色沉淀
结论:淀粉已有水解。
以上三种方案的设计及结论是否正确?如不正确,请简述理由。
Ⅱ.可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去),请填空:
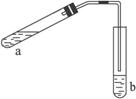
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序操作是______________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是______________________,
(3)实验中加热试管的目的是:
①____________________________________________。
②____________________________________________。
(4)试管b中加有饱和Na2CO3溶液,其作用是_________________________________________。
(5)反应结束后,振荡试管b静置,观察到的现象是___________________________________。
解析:Ⅰ.先分析每种方案的设计是否合理、科学、规范,如不符合要求,则其结论也不可靠;如方案设计合理可行,再评价结论是否正确。方案甲设计正确,但结论不正确。严密的推理是淀粉可能部分水解,也可能一点也没水解,应该进一步做银镜反应或与新制氢氧化铜在加热时的反应,进行进一步的证明;方案乙设计不正确,结论也不正确。因为在酸性条件下,Cu(OH)2与H2SO4反应,而不能与葡萄糖反应。根据上述分析可见,方案丙设计和结论都是正确的。
Ⅱ.本题直接考查乙酸乙酯在实验室中的制取方法。(1)问是对浓硫酸的稀释、安全性考查,浓硫酸与比其密度小的液体混合时一定要先将密度小的液体加到容器中再加浓硫酸。有机物受热时要加入沸石防止暴沸;乙酸和乙醇反应速率慢且生成物浓度小,所以要加热来加快反应速率和蒸出乙酸乙酯,以便使反应物进一步反应。蒸出的乙酸乙酯中会带有乙酸和乙醇,为了得到较纯净的乙酸乙酯,用饱和Na2CO3溶液来反应掉乙酸并溶解乙醇,还可以降低乙酸乙酯在溶液里的溶解度,有利于析出。
答案:Ⅰ.方案甲设计正确,但结论不正确,因为淀粉可能部分水解;方案乙设计不正确,结论也不正确,因为在酸性条件下,Cu(OH)2与H2SO4反应,而不能与葡萄糖反应;方案丙设计和结论都正确。
Ⅱ.(1)先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸
(2)在试管a中加入几粒沸石(或碎瓷片)
(3)①加快反应速率
②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动
(4)吸收随乙酸乙酯蒸出的少量酸性物质和乙醇
(5)b中的液体分层,上层是透明的油状液体

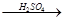 水解液
水解液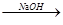 中和液
中和液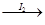 溶液变蓝。
溶液变蓝。
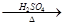 水解液
水解液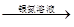 无银镜现象。
无银镜现象。