��Ŀ����
�ô�п��������Fe�����ʣ���ϡ���ᷴӦ�����������Һ�к��д���������п��ͬѧ�����������ķ�Һ����ȡ𩷯��ZnSO4?7H2O������̽�������ʣ���l���Ʊ�𩷯 ʵ����������ͼ��ʾ��

��֪���������������pH��Χ���±���
| �������� | Fe��OH��3 | Fe��OH��2 | Zn��OH��2 |
| ��ʼ����pH | 2.7 | 7.6 | 5.7 |
| ��ȫ����pH | 3.7 | 9.6 | 8.0 |
�ټ�����Լ�a����ѡ��ʹ�õ��У���ˮ��NaClO��Һ��20%��H2O2��Ũ���ᡢŨ����ȣ�Ӧѡ��
�ڼ�����Լ�b����ѡ��ʹ�õ��У�Zn�ۡ�ZnO��Zn��OH��2��ZnCO3��ZnSO4�ȣ�Ӧѡ��
�۴Ӿ���l������2���ù��̵�������
���ڵõ�𩷯ʱ�������м��������ƾ�ϴ�Ӷ�����ˮ��ԭ����
��2��̽��𩷯������
| �¶ȣ��棩 | 60 | 240 | 930 | 1000 |
| ��������������g�� | 19.7 | 16.1 | 8.1 | 8.1 |
��ȡ����ZnSO4?7H2O�����Һ��������μ���NaOH��Һ�������Ȳ�����ɫ�����������ܽ⣮�����ϵ�֪Zn��OH��2�������ԣ���Zn��OH��2����NaOH��Һ�����ӷ���ʽΪ��
���Լ�2������������ҺPH��3.7��Ŀ����������ȫ������������ʵ�鲻�������µ����ʣ�
�۾������½ᾧ�Ĺ����������ᴿ�ķ������ؽᾧ��
��ϴ�Ӿ��������������ӣ�ͬʱ����𩷰�������ʧ��
��2���ݸ���ZnSO4?7H2O���ȵ�1000��ʱ���Ĺ�������������ȷ���ɷ֣�
��������п�������ԣ����Ժ�ǿ�Ӧ������ˮ���Σ�
�ʴ�Ϊ��20%��H2O2���������Һ�е�Fe2+������Fe3+��ͬʱ���������µ����ʣ�
���Լ�2������������ҺPH��3.7��Ŀ����������ȫ������������ʵ�鲻�������µ����ʣ�Zn�ۻ�������õ��������ӻ�ԭ������ȥ�����ã�ZnO��Zn��OH��2��ZnCO3���Է�Ӧ������ҺPH��3.7��ʹ�����ӳ�����ͬʱ�������µ����ʣ�ZnSO4���ܵ�����ҺPH��������������������ӣ�
�ʴ�Ϊ��ZnO��Zn��OH��2��ZnCO3��������Һ��pH��3.7��5.7ʹFe3+ȫ��ת��ΪFe��OH��3������ͬʱ����Zn2+��ʧ�������������ʣ�
�۾����ܽ��ٽᾧ���ᴿ����ķ���Ϊ�ؽᾧ���ʴ�Ϊ���ؽᾧ��
��ϴ�Ӿ��������������ӣ�ͬʱ����𩷰�������ʧ���ڵõ�𩷯ʱ�������м��������ƾ�ϴ�Ӷ�����ˮ��ԭ���ǣ���������ˮ�������ھƾ�������Ŀ����Ϊ�˳�ϴ�����������������ӣ���ֹ�����ܽ⣬Ӱ����ʣ�
�ʴ�Ϊ��Ϊ�˳�ϴ�����������������ӣ���ֹ�����ܽ⣬Ӱ����ʣ�
��2����ZnSO4?7H2O���ȵ�1000��ʱ���Ĺ��������Ϊ8.1g�����ȵ�60��Ὣ���еĽᾧˮʧȥ����1000��ʱ����п�Ѿ��ֽ�Ϊ����п���������ʴ�Ϊ��ZnSO4?7H2O
| ||
| ||
��������п����μ���NaOH��Һ�������Ȳ�����ɫ����������п��Ȼ�������ܽ������������У������Ļ�ѧ��ӦΪ��Zn��OH��2+2OH-=ZnO22-+2H2O��
�ʴ�Ϊ��Zn��OH��2+2OH-=ZnO22-+2H2O��

| Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | Zn��OH��2 | Mn��OH��2 | |
| ��ʼ������pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| ������ȫ��pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
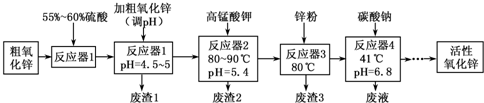
��1��������1������Ҫ�ɷ���
��2����ɡ���Ӧ��2���з�Ӧ֮һ�����ӷ���ʽ��
��3��պȡ����Ӧ��2���е���Һ����
��4��������2���������MnO2��������ȡMnO����֪��
2MnO2��s��+C��s��=2MnO��s��+CO2��g����H=-174.6kJ?mol-1
C��s��+CO2��g��=2CO��g����H=+283.0kJ?mol-1
��д��MnO2��s����CO��g����Ӧ��ȡMnO��s�����Ȼ�ѧ����ʽ��
��5������Ӧ��3���м���п�۵�������
��6������Ӧ��4���õ��ķ�Һ�У����е���Ҫ���ӳ���Na+�⣬����
��7���ӡ���Ӧ��4���о����˵Ȳ����õ���ʽ̼��п��ȡ��ʽ̼��п3.41g����400��450���¼��������أ��õ�ZnO 2.43g�ͱ�״����CO2 0.224L����ʽ̼��п�Ļ�ѧʽΪ
��8�֣�I��ͨ����ұ��������ͭ�Ǵ�ͭ�������ʽ���������п�Ƚ����������������ʣ������Ӧ������������������������Ʒʱ����Ҫ���Ǵ�ͭ��Ϊ��������ͭ��ҺΪ���Һ���õ��ķ���ʵ���˴�ͭ���ᴿ��
�������������γɳ���ʱ��pH
| ���� | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| ��ʼ����ʱ��pH | 7.6 | 2.7 | 5.7 | 4.7 |
| ��ȫ����ʱ��pH | 9.7 | 3.7 | 8.5 | 7.3 |
��2���ھ���ͭ�Ĺ����У�Cu2+Ũ�����ͣ�c(Fe2+)��c(Zn2+)�������������趨ʱ��ȥ���е�Fe2+��Zn2+����ͬѧ��������³������̣�

|
�ڲ������� �������ϱ����ݷ��������ӷ������ܹ���ȥ�����ʽ�����������
���ѧʽ����
II���ؽ������ӶԺ�������Ȼ�������ص���Ⱦ��ij�����������ķ�ˮ��pH=2.0���ܶ�Ϊ1g��mL-1���к���Ag+��Pb2+���ؽ������ӣ���Ũ��ԼΪ0.01mol��L-1���ŷ�ǰ���ó��������������ֽ����������й��������£�
| ���ܵ���� | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3��10-17 | 5.6��10-8 | 6.3��10-50 | 7.1��10-9 | 1.2��10-15 | 3.4��10-28 |
a��NaOH b��Na2S c��KI d��Ca��OH��2
��2���������ʯ�Ҵ���������ˮ��ʹ��Һ��pH=8.0��������ķ�ˮ��c(Pb2+)=
�ô�п��������Fe�����ʣ���ϡ���ᷴӦ������ʱ�����Һ�к��д���������п��ͬѧ���ø÷�Һ����ȡ𩷯��ZnSO4��7H2O���� �Ʊ�𩷯��ʵ����������ͼ��ʾ��
![]()

![]()
![]() ��֪���������������pH��Χ���±���
��֪���������������pH��Χ���±���
�������� | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
��ʼ����pH | 2��7 | 7��6 | 5��7 |
��ȫ����pH | 3��7 | 9��6 | 8��0 |
![]() ��ش��������⣺
��ش��������⣺
![]() �� ��1����ѡ����Լ�a�У���ˮ��NaClO��Һ��20����H2O2��Ũ���ᡢŨ����ȣ�Ӧѡ�������� ������������������������������������������ ��
�� ��1����ѡ����Լ�a�У���ˮ��NaClO��Һ��20����H2O2��Ũ���ᡢŨ����ȣ�Ӧѡ�������� ������������������������������������������ ��
![]() �� ��2�� ��ѡ����Լ�b�У� Zn�ۡ�ZnO��Zn(OH)2��ZnCO3��ZnSO4�ȣ�Ӧѡ���������� �������������������������������������������������� �������������� ��
�� ��2�� ��ѡ����Լ�b�У� Zn�ۡ�ZnO��Zn(OH)2��ZnCO3��ZnSO4�ȣ�Ӧѡ���������� �������������������������������������������������� �������������� ��
![]() �� ��3������l������2�������������������������� ��
�� ��3������l������2�������������������������� ��
![]() �� ��4���ڵõ�𩷯ʱ�������м��������ƾ�ϴ�Ӷ�����ˮ��ԭ������������ ��
�� ��4���ڵõ�𩷯ʱ�������м��������ƾ�ϴ�Ӷ�����ˮ��ԭ������������ ��
![]()