题目内容
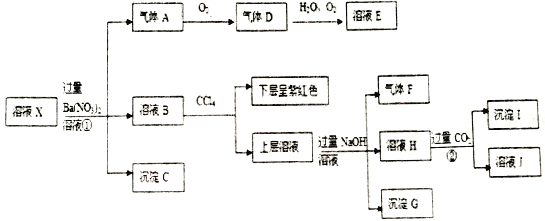
【题目】现有中学化学常见三种金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙______________、H______________。
(2)写出反应⑤的离子方程式:__________________________________________。
(3)D溶液与F溶液反应,生成沉淀,该沉淀的化学式为_____________,该沉淀在空气中由白色很快变为灰绿色最后变为红褐色,该反应的化学方程式为______________。
(4)物质C与物质E的溶液反应生成5.6 L氢气(标准状况)时,参与反应的物质C的质量是_______克。
【答案】 Cl2 Fe(OH)3 2Fe2++Cl2=2Fe3++2Cl- Fe(OH)2 4Fe(OH)2+O2+2H2O=4Fe(OH)3 14
【解析】金属单质A焰色反应为黄色,故A为金属Na,与水反应生成NaOH与氢气,则D为NaOH,气体甲为H2;B是地壳中含量最多的金属,氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀H是Fe(OH)3,故物质G中含有Fe3+,金属C与盐酸反应生成F,F与氯气反应生成G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3.
(1)气体乙的化学式:Cl2,H为Fe(OH)3;
(2)反应⑤的离子方程式为Fe2++Cl2=2Fe3++2Cl-;
(3)物质D与物质F的溶液反应生成沉淀的化学式为Fe(OH)2,该沉淀在空气中从白色很快变为灰绿色最后变为红褐色,该反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)Fe与稀盐酸生成5.6 L氢气(标准状况),氢气的物质的量为0.25mol,则Fe的物质的量为0.25mol,质量为56g/mol×0.25mol=14g。

【题目】下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe 2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-= Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-= Al(OH)3↓ |
A. A B. B C. C D. D