题目内容
【题目】苯乙烯是重要的基础有机化工原料.工业中以乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:C6H5-CH2CH3(g)![]() C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
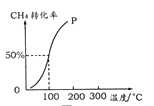
(1)向体积为VL的密闭容器中充入n mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:
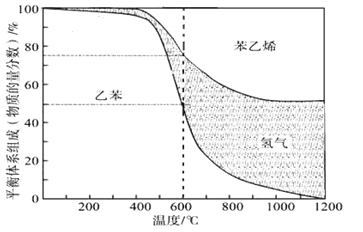
600℃时,该反应的平衡常数_____________。
(2)乙苯在特定催化剂下发生氧化脱氢:
C6H5-CH2CH3(g)+1/2O2(g)![]() C6H5-CH=CH2(g)+H2O(g) ΔH1
C6H5-CH=CH2(g)+H2O(g) ΔH1
已知 H2的燃烧热ΔH= b kJ/mol,水的汽化热为c J/g,则 ΔH1=____________。
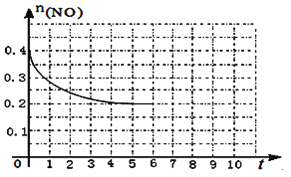
(3)在汽车上安装三元催化转化器可实现反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
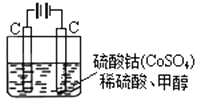
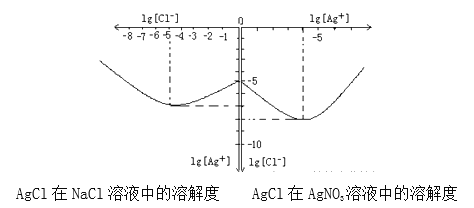
(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl+Cl-═[AgCl2]-,如图是某温度下AgCl在NaCl溶液中的溶解情况.
由以上信息可知:
①由图知该温度下AgCl的溶度积常数为_________。
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:_______________。
【答案】 n/6V (a+b+0.018c)kJ·mol―1 低温 作图如图所示: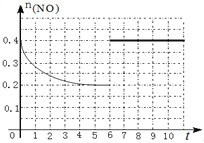 10-12 开始Cl—抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl—浓度增大使AgCl形成[AgCl2]-络合物,所以Ag+浓度又变大了。
10-12 开始Cl—抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl—浓度增大使AgCl形成[AgCl2]-络合物,所以Ag+浓度又变大了。
【解析】(1)①C6H5-CH2CH3(g)C6H5-CH=CH2(g)+H2(g)起始量a mol0 0变化量x molx mol x mol平衡量 (a-x)mol x mol x mol 由图1可知,600℃时乙苯的含量为50%,则: ![]() ×100%=50%,解得x=
×100%=50%,解得x=![]() a,
a,
各物质的平衡浓度:c(C6 H5-CH2 CH3 )=![]() molL-1,c(C6 H5-CH=CH2)=
molL-1,c(C6 H5-CH=CH2)=![]() molL-1,c(H2)=
molL-1,c(H2)=![]() molL-1,则K=
molL-1,则K=![]() ;
;
(2)H2的燃烧热(△H)分别为bkJ.molL-1,可得热化学方程式:①H2(g)+![]() O2(g)=H2O(l)△H=bkJ/mol,水的汽化热为c焦耳/克,则为0.018ckJ/mol,可得:②H2O(l)=H2O(g)△H=0.018ckJ/mol已知③:C6H5-CH2CH3(g)C6H5-CH=CH2(g)+H2(g)△H1=akJmol-1根据盖斯定律,③+①+②可得:C6H5-CH2CH3(g)+
O2(g)=H2O(l)△H=bkJ/mol,水的汽化热为c焦耳/克,则为0.018ckJ/mol,可得:②H2O(l)=H2O(g)△H=0.018ckJ/mol已知③:C6H5-CH2CH3(g)C6H5-CH=CH2(g)+H2(g)△H1=akJmol-1根据盖斯定律,③+①+②可得:C6H5-CH2CH3(g)+![]() O2(g)C6H5-CH=CH2(g)+H2O(g),故△H=akJmol-1+bkJ/mol+0.18ckJmol-1=(a+b+0.018c)kJmol-1;
O2(g)C6H5-CH=CH2(g)+H2O(g),故△H=akJmol-1+bkJ/mol+0.18ckJmol-1=(a+b+0.018c)kJmol-1;
(3)2NO(g)+2CO(g)N2(g)+2CO2(g)△H<0,反应前后气体体积减小△S<0,低温下满足△H-T△S<0,即在低温时反应自发进行;/span>
已知反应为2NO(g)+2CO(g)N2(g)+2CO2(g),2L密闭容器中充入NO、CO各0.4mol,达到平衡时NO为0.2mol, 2NO(g)+2CO(g)N2(g)+2CO2(g) 起始(mol):0.4 0.4 0 0转化(mol):0.2 0.2 0.1 0.2平衡(mol):0.2 0.2 0.1 0.2
则K=![]() =5;第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,则c(NO)=
=5;第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,则c(NO)=![]() =0.2mol/L,c(CO)=
=0.2mol/L,c(CO)=![]() =0.2mol/L,c(N2)=
=0.2mol/L,c(N2)=![]() =0.2mol/L,c(CO2)=
=0.2mol/L,c(CO2)=![]() =0.2mol/L,Qc=
=0.2mol/L,Qc=![]() =5=K,说明是平衡状态,所以第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,仍是平衡状态,但是NO的物质的量变为原来的2倍,作图为
=5=K,说明是平衡状态,所以第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,仍是平衡状态,但是NO的物质的量变为原来的2倍,作图为 ;
;
(4)当c(Ag+)=10-5mol/L时,c(Cl-)=10-7mol/L,所以AgCl的溶度积常数Ksp=c(Ag+)c(Cl-)=10-5mol/L10-7mol/L=10-12(mol/L)2;(2)根据沉淀溶解平衡:AgCl(s)=Cl-(aq)+Ag+(aq),将氯化银放在氯化钠中,Cl-抑制了AgCl的溶解,但Cl-浓度增大使AgCl形成络合物:AgCl+Cl-═[AgCl2]-。

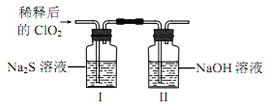
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(l)ClO2的制备:(已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4)

①装置A中反应的化学方程式为_______________。
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为 a→_________(按气流方向,用小写字母表示)
③装置D的作用是_________。
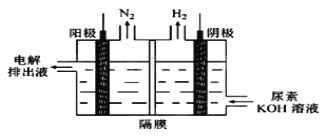
(2)ClO2与 Na2S 的反应
将上述收集到的ClO2用 N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
操作步骤 | 实验现象 | 结论 |
取少量Ⅰ中溶液于试管甲中, 加入Ba(OH)2溶液,振荡 | ①_________ | 有硫酸根离子生成 |
另取少量Ⅰ中溶液于试管乙中, 滴加品红溶液和盐酸 | 品红溶液不翅色 | ② 无_____生成 |
若在试管甲中继续加Ba(OH)2溶液至 过量,静置,取上层清液于试管丙③______ | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为__________。用于处理含硫废水时,ClO2相对于Cl2的优点是____________(任写2条)。
【题目】海水是巨大的资源宝库。下图是实验室模拟工业从海水资源获取某些重要化工原料的流程示意图。

回答下列问题:
(1)由于溴离子在海水中浓度很低(0.067g/L),要进行溴元素的浓缩、富集。实验室若要直接浓缩海水时,下面的仪器肯定不需要的是(填编号)__________
A.玻璃棒 B.三脚架 C.坩埚 D.蒸发皿 E.酒精灯
(2)要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是___________。
A.分析氯化钠含量 B.测定溶液密度 C.观察是否有沉淀析出
(3)写出溴水中通入SO2时反应的离子方程式____________。
(4)上图中虚线框内流程也可用![]() Na2CO3溶液吸收Br2的反应化学方程式补充完整:
Na2CO3溶液吸收Br2的反应化学方程式补充完整:
____Br2 + _____Na2CO3 = _____NaBrO3 +___________ +________
(5)现有一份吸收了溴的无色溶液(采用上述两种方法之一,且吸收剂和溴恰好完全反应),请你通过实验探究该溶液究竟是采用那种方法吸收溴的。
① 提出合理假设
假设1:采用纯碱吸收法,吸收液中含大量Na+、Br –、BrO3-
假设2:_____________________________________________。
② 设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论。限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管;无水乙醇、苯、0.10mol/LAgNO3、0.10mol/LBaCl2、2mol/LHCl 查资料得:Ba(BrO3)2为白色固体,微溶于水
实验步骤 | 预期现象和结论 |
步骤1:用量筒取样品溶液2mL分别于A、B试管中,往A试管中加入___________。 | 若____________________________,则假设1一定能成立。 |
步骤2:往试管B中加入___________。 | 若_________________,则假设2一定能成立。 |