题目内容
某混合气体由两种气态烃组成.2.24L该混合气体完全燃烧后,得到4.48L二氧化碳(气体已折算成标准状况)和3.6g水.则这两种气体可能是( )
| A、CH4和C3H8 |
| B、CH4和C3H4 |
| C、C2H4和C3H4 |
| D、C2H4和C2H6 |
考点:有关有机物分子式确定的计算
专题:有机物分子组成通式的应用规律
分析:2.24L该混合气体的物质的量为0.1mol,完全燃烧得到4.48L二氧化碳和3.6g水,生成二氧化碳的物质的量为0.2mol,水的物质的量为0.2mol,则混合气体平均分子式为C2H4,利用平均值法判断.
解答:
解:2.24L该混合气体的物质的量=
=0.1mol,完全燃烧得到4.48L二氧化碳和3.6克水,生成二氧化碳的物质的量=
=0.2mol,水的物质的量=
=0.2mol,则混合气体平均分子式为C2H4,
A.CH4和C3H8混合,平均H原子数目介于4~8之间,不可能为4,故A不符合;
B.CH4和C3H4按照1:1混合,平均分子式为C2H4,故B符合;
C.C2H4和C3H4混合,平均C原子数目介于2~3之间,不可能为2,故C不符合;
D.C2H4和C2H6混合,以任意比混合,平均C原子数目都是2,平均H原子数目介于4~6之间,不可能为4,故D不符合;
故选B.
| 2.24L |
| 22.4L/mol |
| 4.48L |
| 22.4L/mol |
| 3.6g |
| 18g/mol |
A.CH4和C3H8混合,平均H原子数目介于4~8之间,不可能为4,故A不符合;
B.CH4和C3H4按照1:1混合,平均分子式为C2H4,故B符合;
C.C2H4和C3H4混合,平均C原子数目介于2~3之间,不可能为2,故C不符合;
D.C2H4和C2H6混合,以任意比混合,平均C原子数目都是2,平均H原子数目介于4~6之间,不可能为4,故D不符合;
故选B.
点评:本题考查分子式的确定、混合物计算,题目难度中等,关键是利用平均分子组成判断烃的组成,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、在反应KIO3+6 HI=KI+3I2十3 H2O中,每生成3mo1 I2转移的电子数为5NA |
| B、100mL 18.4mo1?L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C、1 L 0.1 moI?L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA |
| D、将0.lmol FeC13滴人沸水中可制得0.1NA Fe(OH)3胶粒 |
常温下把氨水滴到盐酸中,当c(NH4+)=c(Cl-)时,混合液的pH值( )
| A、等于7 | B、大于7 |
| C、小于7 | D、无法判断 |
常温下,下列对醋酸稀溶液的叙述中,正确的是( )
A、将pH=a的醋酸稀释变为pH=a+1,醋酸的浓度则变为原来的
| ||
B、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| C、pH=a的醋酸与pH=a+1的醋酸分别中和等物质的量的NaOH溶液,二者所消耗体积比为1:10 | ||
| D、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,存在a+b=14 |
下列有关物质分类或归类正确的是( )
①化合物:CaCl2、烧碱、聚苯乙烯、HD
②碱性氧化物:Na2O、CuO、Al2O3、FeO
③电解质:水、胆矾、冰醋酸、氢氧化镁
④酸性氧化物:CO2、SO2、NO2、P2O5
⑤有机物:酒精、甲烷、蔗糖、蛋白质.
①化合物:CaCl2、烧碱、聚苯乙烯、HD
②碱性氧化物:Na2O、CuO、Al2O3、FeO
③电解质:水、胆矾、冰醋酸、氢氧化镁
④酸性氧化物:CO2、SO2、NO2、P2O5
⑤有机物:酒精、甲烷、蔗糖、蛋白质.
| A、①③④ | B、②④ |
| C、②③④ | D、③⑤ |
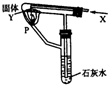 按如图的装置持续通入X气体并在支管P处点燃,实验时澄清石灰水变浑浊,则X、Y可能是( )
按如图的装置持续通入X气体并在支管P处点燃,实验时澄清石灰水变浑浊,则X、Y可能是( )| A、氢气和碳酸钠 |
| B、一氧化碳和碳酸钠 |
| C、一氧化碳和氧化铜 |
| D、氢气和氧化铁 |
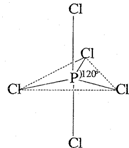 2014年3月9日凌晨,一辆拖挂车装载150桶约30吨白磷驶往山东,在雅西高速西昌收费站附近发生侧翻,车上白磷泄漏燃烧,大量白色烟雾飘进西昌城区.
2014年3月9日凌晨,一辆拖挂车装载150桶约30吨白磷驶往山东,在雅西高速西昌收费站附近发生侧翻,车上白磷泄漏燃烧,大量白色烟雾飘进西昌城区.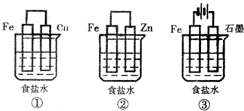
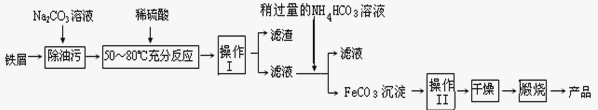
 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题: