题目内容
某化学兴趣小组的同学在学习了《铝 金属材料》一节后,产生了浓厚的实验探究兴趣,欲对铝热反应进行实验探究。下面是他们活动的一则案例,请你帮助完成相关的内容,回答有关问题。
实验目的
1.观察铝热反应的现象,认识铝的还原性及其应用。
2.提高设计实验方案的能力及观察问题、分析问题的能力,增强实验探究意识。
实验原理
铝具有较强的还原性,在高温下,能把没有它活泼的金属从其氧化物中还原出来。
金属氧化物+铝 金属+氧化铝
金属+氧化铝
还原性:铝>金属
仪器和药品
蒸发皿、铁架台(带铁圈)、小试管、烧杯、药匙、坩埚钳、镊子、剪刀、火柴、砂纸、滤纸、长铁钉、砂子、三氧化二铁、铝粉、镁条、氯酸钾。
实验预测
铝是一种活泼金属,可能与其他金属的氧化物发生置换反应。
实验操作
甲同学在如图所示装置中加入药品(蒸发皿内盛有砂子)。
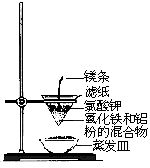
该同学引发铝热反应的实验操作是__________________。
实验现象
上述实验观察到的现象是_______________。
实验结论
在高温下,铝与氧化铁反应,放出大量的热。反应的化学方程式为_______________。
提出问题
乙同学对该实验进行了分析,发现存在几点明显不足:
1.因滤纸的遮挡、燃烧生成大量的烟和反应速率过快等而不易观察清楚红热现象。
2.铁珠四溅,容易发生事故。
实验改进
实验小组的同学积极思考,对实验进行了改进,取得了良好的效果。其改进实验如下: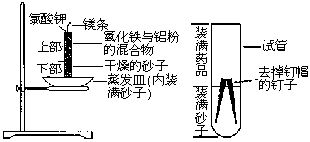
如上图所示连好装置,加好药品。其中蒸发皿中盛满砂子(用水润湿),在小试管内装入1/3干燥的砂子。用镊子向砂子中插入两支去掉钉帽的铁钉,将铁钉约1/4部分留在砂子外并用镊子将其靠紧。在砂子上面装满氧化铁和铝粉的混合物。在小试管上部放入少量氯酸钾粉末,并在其中插入一根镁条,点燃镁条。反应完全后,用坩埚钳夹住小试管的上端并将其敲断,倒出砂子并取出已焊接在一起的两支铁钉。
观察与思考
1.实验中氯酸钾和镁条的作用是什么?
2.你认为改进后的实验具有的优点是:_______________。
3.铝热反应有什么用途?
加少量KClO3,插上镁条并将其点燃; “纸漏斗”内混合物立即剧烈反应,发出耀眼的光芒,产生大量的烟。“纸漏斗”被烧破,有红热状态的液珠落入蒸发皿内的细砂上。液珠冷却后变为黑色固体; Fe2O3+2Al Al2O3+2Fe);
Al2O3+2Fe);
1.实验中氯酸钾和镁条的作用:镁条引燃,氯酸钾做氧化剂,且分解产生的氧气助燃镁条,使温度升高,引发铝热反应。即氯酸钾和镁条做铝热反应的引发剂。
2.(1)现象明显:由于试管透明,当反应开始后,容易观察到以下现象:①整个红热过程以及铁水生成和自上而下的熔化流动;②红热的铁水将部分埋在铝热剂中的铁钉焊接在一起。
(2)成功率高、安全性好:实验过程中无铁珠迸溅
3.铝热反应的用途:(1)焊接钢轨;(2)冶炼活泼性比铝弱的难熔金属如钒、铬、锰等;(3)定向爆破;(4)军事等。]
【试题分析】

 阅读快车系列答案
阅读快车系列答案