题目内容
在t°C时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如下图所示。
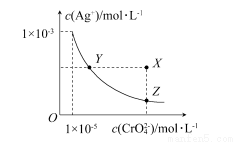
又知AgCl的Ksp=1.8×10-10。
下列说法不正确的是( )
A.t°C时,Ag2CrO4的Ksp为1×10-8
B.在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t°C时,Y点和Z点的Ag2CrO4的Ksp相等
D.t°C时,将0.01 mol·L-1 AgNO3溶液滴入20 mL 0.01 mol·L-1 KCl和0.01 mol·L-1 K2CrO4的混合溶液中,Cl-先沉淀
A
【解析】由图中数据可计算得Ksp[Ag2CrO4]=[Ag+]2·[CrO42—]=1.0×10-11,可知A错误;在Ag2CrO4溶液中加入K2CrO4,c(CrO42—)增大,则c(Ag+)降低,而X点与Y点的c(Ag+)相同,所以B正确;Y点、Z点溶液的温度相同,则Ksp相同,C正确;由AgCl的Ksp计算此条件下AgCl沉淀时的c(Ag+)=1.8×10-8 mol·L-1,由Ag2CrO4的Ksp计算得Ag2CrO4沉淀时的c(Ag+)≈3.16×10-5mol·L-1,可知Cl-优先沉淀。

 名校课堂系列答案
名校课堂系列答案某研究性学习小组为了探究醋酸的电离情况,进行了如下实验:
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、________和________。
(2)为标定某醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
则该醋酸溶液的准确浓度为________。(保留小数点后四位)
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如下:
醋酸浓度(mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:____________________。
(2)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将________。(填“增大”“减小”或“不变”)
实验三 探究温度对醋酸电离程度的影响
请你设计一个实验完成该探究,请简述你的实验方案:____________。


