��Ŀ����
����Ŀ��̼�����㷺�طֲ�����Ȼ���У�̼�����Ļ����������������ڹ�ҵ�����ͿƼ���������Ҫ��;��
��1�������裨Si3N4����һ�������մɲ��ϣ�������SiO2�������̿��1300��1700��C�ĵ������з�Ӧ�Ƶã�3SiO2(s) + 6C(s) + 2N2(g)![]() Si3N4(s) + 6CO(g) ��H����1591.2 kJ��mol��1����÷�Ӧÿת��1mol e�����ɷų�������Ϊ ��
Si3N4(s) + 6CO(g) ��H����1591.2 kJ��mol��1����÷�Ӧÿת��1mol e�����ɷų�������Ϊ ��
��2��ij�о�С���ֽ�����CO(g) ��H2O(g) �Ļ������ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У�һ�������·�����Ӧ��CO(g) + H2O(g) ![]() CO2(g) + H2(g)���õ��������ݣ�
CO2(g) + H2(g)���õ��������ݣ�
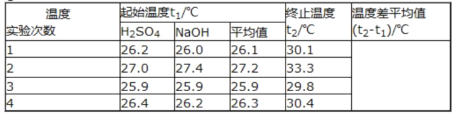
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | ��ƽ������ʱ��/min | ||
CO | H2O | CO | H2 | |||
1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
2 | 900 | 1 | 2 | 0.5 | 0.5 | |
�� ʵ��1�У�ǰ5min�ķ�Ӧ����v(CO2) �� ��
�� �������ж�ʵ��2�Ѿ��ﵽƽ��״̬���� ������ţ���
a��������CO��H2O��CO2��H2��Ũ�Ȳ��ٱ仯
b��������ѹǿ���ٱ仯
c�����������ܶȱ��ֲ���
d��v��(CO)��v��(CO2)
e�������������ƽ����Է�����������ʱ����仯
�� ��ʵ��2�������Ǿ��ȵ��ܱ�������ʵ����H2O(g) ��ת������(H2O)��ʱ��仯��ʾ��ͼ��ͼ1��ʾ��b��v�� v������������������� ����������t3��t4ʱ�̣�H2O(g) ��ת������(H2O)���͵�ԭ���� ��

��3������CO��H2��ֱ�Ӻϳɼ״�����ͼ���ɡ��״�-�������γɵ���ɫȼ�ϵ�صĹ���ԭ��ʾ��ͼ��ͼ2��д����ʯīΪ�缫�ĵ�ع���ʱ�����ĵ缫��Ӧʽ �����øõ�ص��1L 0.5mol��L��1��CuSO4��Һ�����������560mLO2����״���£�ʱ��������Һ��pH�� ����Һ���ǰ������ı仯���Բ��ƣ���
���𰸡���1��132.6 kJ����2����0.15 mol��L��1��min��1����ad ���������÷�Ӧ�ﵽƽ�������ӦΪ���ȷ�Ӧ�ҷ�Ӧ����Ϊ�������������������¶����ߣ�ƽ�������ƶ�����3��CH3OH ��6e�� + H2O = CO2 �� + 6H+��1��
��������
�����������1�����ݷ�Ӧ����ʽ��ת�Ƶ���12mol���ų�����1591.2kJ����ת��1mol���ӣ��ų�����Ϊ1591.2/12kJ=132.6kJ��(2)�����ݷ�Ӧ����ʽ������CO2�����ʵ���Ϊ1.5mol�����ݻ�ѧ��Ӧ���ʵı���ʽ��v(CO2)=0.15/(2��5)mol/(L��min)=0.015mol/(L��min)����a�����ݻ�ѧƽ��״̬�Ķ��壬����ֵ�Ũ�Ȳ��ٸı䣬˵����Ӧ�ﵽƽ�⣬����ȷ��b����Ӧǰ������ϵ��֮����ȣ����ѹǿ���䣬����˵����Ӧ�ﵽƽ�⣬�ʴ���c�������ܶȶ��壬��ֶ������壬���������������䣬�����Ǻ��ݣ�����������䣬����ܶȲ��䣬����˵����Ӧ�ﵽƽ�⣬�ʴ���d���ò�ͬ���ʵķ�Ӧ���ʣ���ʾ�ﵽ��ѧƽ�⣬Ҫ��Ӧ������һ��һ�棬�ҷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�v��(CO)˵����Ӧ������Ӧ������У�v��(CO2)˵����Ӧ���淴Ӧ������У�����������֮�ȵ���1��1������ȷ��e������ƽ��Ħ�������Ķ��壬�������ʵ������䣬��Ӧǰ������ϵ��֮����ȣ����������ʵ������䣬���ƽ��Ħ���������䣬����˵����Ӧ�ﵽƽ�⣬�ʴ�����b�㷴Ӧû�дﵽƽ�⣬������Ӧ������У����v��>v�棻�÷�Ӧ�ﵽƽ�������ӦΪ���ȷ�Ӧ�ҷ�Ӧ����Ϊ�������������������¶����ߣ�ƽ�������ƶ���(3)����Ӧ��ʧȥ���ӣ����ϼ����ߣ����ͨ�״�һ��Ϊ����������ͼ2����������H������˵缫��ӦʽΪ��CH3OH ��6e�� + H2O = CO2 �� + 6H�������������ӦʽΪO2��4H����4e��=2H2O��������ӦʽΪ2H2O��4e��=O2����4H�������ݵ�ʧ������Ŀ�غ㣬����O2��4e����4H����n(H��)=4��560��10��3/22.4mol=0.1mol��c(H��)=0.1/1mol��L��1=0.1mol��L��1����pH=1��

 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�����Ŀ���������ʷ������ȷ������� ��
�� | �� | �� | ���������� | |
A | ���� | ���� | �ռ� | ������̼ |
B | �ռ� | ���� | ʳ�� | һ����̼ |
C | ������ | ���� | ʯ��ʯ | ˮ |
D | ���Լ� | ���� | �մ� | �������� |