题目内容
某混合物A含有明矾、Al2O3、CuO,在一定条件下可实现如下图所示的物质之间的转化:
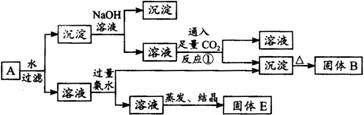
据此判断:
(1)固体B所含物质的化学式为________。
(2)固体E所含物质的化学式为________。
(3)反应①的离子方程式为________。
(1)Al2O3 (2)(NH4)2SO4、K2SO4
(3)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
【解析】加入水后,沉淀是Al2O3、CuO,Al2O3是两性氧化物,溶于NaOH溶液生成NaAlO2,NaAlO2+CO2+ 2H2O=Al(OH)3↓+NaHCO3,2Al(OH)3 Al2O3+3H2O,KAl(SO4)2溶于水完全电离:KAl(SO4)2=K++Al3++2SO42-,Al3++3NH3·H2O=A1(OH)3↓+3NH4+,溶液中的离子组成为NH4+、K+、SO42-,从而得出正确答案。
Al2O3+3H2O,KAl(SO4)2溶于水完全电离:KAl(SO4)2=K++Al3++2SO42-,Al3++3NH3·H2O=A1(OH)3↓+3NH4+,溶液中的离子组成为NH4+、K+、SO42-,从而得出正确答案。

(1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________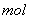 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________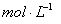 。
。
|
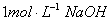 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。 ①合金中镁的质量 g。
②盐酸的物质的量浓度 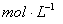 。
。