题目内容
向50mL Na2SO4和Na2CO3的混合液中加入过量BaCl2溶液,得到14.51g白色沉淀.向白色沉淀中加过量稀硝酸,充分反应后,沉淀减少到4.66g,并有气体放出.试计算:
(1)原混合液中Na2SO4和Na2CO3的物质的量浓度.
(2)产生的气体在标准状况下的体积.
答案:
解析:
解析:
|
解: (1)依题:n(BaSO4)= n(BaCO3)= 由Na2SO4~BaSO4,Na2CO3~BaCO3~CO2 知c(Na2CO3)= c(Na2SO4)= (2)V(CO2)=22.4×0.05=1.12L. |

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
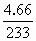 =0.02mol,
=0.02mol,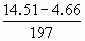 =0.05mol.
=0.05mol.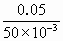 =1mol/L,
=1mol/L,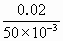 =0.4mol·L-1.
=0.4mol·L-1.