��Ŀ����
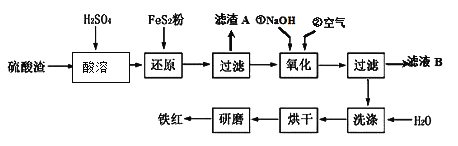
����Ŀ�����仯�����ڹ�ҵ����������;�����������Ҫ�ɷ�ΪMg2B2O5��H2O��Fe3O4����������Fe2O3��FeO��CaO��Al2O3��SiO2��)Ϊԭ���Ʊ�����(H3BO3)�Ĺ���������ͼ��ʾ��

�ش��������⣺
��1��д��Mg2B2O5��H2O�����ᷴӦ�Ļ�ѧ����ʽ_____________��Ϊ��߽������ʣ����ʵ���������Ũ��Ũ���⣬���ɲ�ȡ�Ĵ�ʩ��_________��д����������
��2������ �Ĵ��ԣ��ɽ�������������з��롣���������л�ʣ���������______��д��ѧʽ����
��3�����������������ȼ�H2O2��Һ��������_______�� Ȼ���ٵ�����Һ��pHԼΪ5��Ŀ����________��
��4�������������е���Ҫ������ �������ƣ���
��5��������Ϊԭ�Ͽ��Ƶ����⻯�ƣ�NaBH4���������л��ϳ��е���Ҫ��ԭ���������ʽΪ_______��
��6����������������ɾ������������������֡�������ͽ���þΪԭ�Ͽ��Ʊ��������û�ѧ����ʽ��ʾ�Ʊ�����___________��
���𰸡���1�� Mg2B2O5��H2O+2H2SO4![]() 2MgSO4+2H3BO3����С��������������߷�Ӧ�¶ȡ�
2MgSO4+2H3BO3����С��������������߷�Ӧ�¶ȡ�
��2�� Fe3O4�� SiO2��CaSO4��
��3����Fe2+����ΪFe3+��ʹAl3+��Fe3+�γ������������ȥ��
��4������ˮ������þ
��5��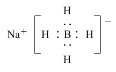
��6�� 2H3BO3 ![]() B2O3+3HO B2O3+3Mg
B2O3+3HO B2O3+3Mg ![]() 3MgO+2B
3MgO+2B
����������1����д��ѧ����ʽ���Ƿ��ռ�ʽ̼���κ���ķ�Ӧ������Ҫ�ȷ���Mg2B2O5��H2O ����Ԫ�صĻ��ϼ�Ϊ+3�ۣ���ϵ������ͼ���ղ������֪����Ԫ�ر�ΪH3BO3��H3BO3Ϊ���ᣬ������ˮ�����ⲻ��������ԭ��Ӧ����þԪ��ת��Ϊ����þ���ӿ췴Ӧ���ʿ��Բ������µȴ�ʩ�������������ĽӴ����Ҳ����ѧ���档
��2����ϵ���д���ֻ��Fe3O4������дFe3O4����ѧ��ѧ��Ӧ�������ſ�������ʣ�µIJ��������SiO2����CaSO4��
��3���Ƚ���Һ�е�Fe2+����ΪFe3+���ٵ�����Һ��pH���Գ�ȥ��Һ�е�Al3+��Fe3+�����Ǹ�������ѵ���ij��ӷ�����
��4�����н���������þ��ĸҺ��Ӧ�������뵽����þҲ��ᾧ������ֻ�Ǿ��庬���߸��ᾧˮ�������뵽������ˮ����п����ˮ�����������룩��������þ����Ӧ��Ҳ���ԡ�
��5�����⻯�Ƶĵ���ʽ�ܲ����棬����ʽ�������Ӽ����������ڲ��Ĺ��ۼ������ֺϳɡ�
��6������ʱ�����룬�����Ӧ���¶�Ӧ�ñȽϸߣ�����H3BO3��ֽ⣬Ȼ������û���Ӧ���ٽ���ѧ����ʽ��ƽ�ͺá�