题目内容
5.有一真空储气瓶,净重500克.在相同条件下,装满氧气后重508克,装满另一种气体x 时重511 克,则 x 的相对分子质量为( )| A. | 44 | B. | 48 | C. | 64 | D. | 71 |
分析 氧气的质量为508g-500g=8g、X的质量为511g-500g=11g,氧气体积与气体X的体积相等,相同条件下二者物质的量相等,根据n=$\frac{m}{M}$计算氧气物质的量,再根据M=$\frac{m}{n}$计算X的相对分子质量.
解答 解:氧气的质量为508g-500g=8g,则氧气物质的量为$\frac{8g}{32g/mol}$=0.25mol,
氧气体积与气体X的体积相等,相同条件下二者物质的量相等,X的质量为511g-500g=11g,故X的摩尔质量为$\frac{11g}{0.25mol}$=44g/mol,故X的相对分子质量为44,
故选:A.
点评 本题考查阿伏伽德罗定律及其推论,比较基础,注意根据PV=nRT理解掌握阿伏伽德罗定律及其推论.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. | 待测液中加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,则待测液中一定有硫酸根离子 | |
| B. | 用灼烧的方法可鉴别丝绸与棉布 | |
| C. | 无色溶液中加入Na2CO3溶液产生白色沉淀,则该无色溶液中含有Ca2+ | |
| D. | 待测液中加入AgNO3溶液,有白色沉淀生成,则待测液中含有Cl- |
20.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2 L N2含有的分子数为0.5 NA | |
| B. | 10克Ne所含原子数约为6.02×1023 | |
| C. | 在同温同压时,相同体积的任何气体所含的原子数相同 | |
| D. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA |
10.已知 I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<H2O2<Fe2+<I-<SO2,则下列反应不能发生的是( )
| A. | 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ | B. | I2+SO2+2H2O=H2SO4+2HI | ||
| C. | 2Fe3++2I-=2Fe2++I2 | D. | H2O2+H2SO4=SO2+O2+2H2O |
17.将5mol•L-1HCl溶液和1mol•L-1HCl溶液混合,配制2mol•L-1HCl溶液,请问需要5mol•L-1HCl溶液和1mol•L-1HCl溶液的体积之比是:(设混合后溶液的体积等于混合前两种溶液体积之和)( )
| A. | 1:3 | B. | 3:1 | C. | 1:4 | D. | 4:1 |
14.下列有关SO2的性质的探究实验报告记录的实验现象正确的是( )
| 实验 | 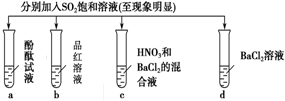 | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色溶液 | |
| C | 无色 | 无色 | 白色沉淀 | 无色溶液 | |
| D | 红色 | 无色 | 白色沉淀 | 白色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
15.下列物质的水溶液,滴加稀硫酸或氯化镁溶液时,均有白色沉淀生成的是( )
| A. | BaCl2 | B. | NaHCO3 | C. | Ba(OH)2 | D. | NaOH |