题目内容
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,思考扇形元素周期表的填充规律,下列说法正确的是( )
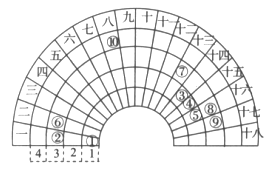
A. ②、⑧、⑨对应简单离子半径依次减小
B. 该表中标注的元素全部是主族元素
C. 元素⑥和⑦的原子序数相差11
D. ④的最高价氧化物对应的水化物能与其氢化物反应
【答案】D
【解析】由元素在周期表中的位置可以知道,①为H、②为Na、③为C、④为N、⑤为O、⑥为Mg、⑦为Al、⑧为S、⑨为Cl、⑩为Fe,A.因为②为Na、⑧为S、⑨为Cl电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Cl->Na+,故A错误;
B.因为⑩为Fe,为副族元素,故B错误;C. 元素⑥为Mg元素⑦为Al,两原子序数相差1。故C错;D. ④的最高价氧化物对应的水化物为HNO3,其氢化物为NH3两者可以发生反应,故D正确。

练习册系列答案
相关题目