题目内容
【题目】工业纯碱中常含NaCl,某活动小组设计如图装置测定工业纯碱中Na2CO3的含量。
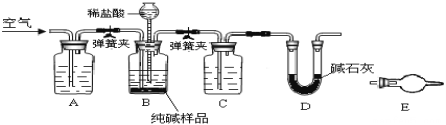
(1)检验装置B气密性方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量水,使漏斗内水面高于瓶内水面,停止加水后,若___________,说明装置不漏气。
(2)装置A的作用是_______,装置C中的试剂为_______。
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?_______(选填“必要”或“不必要”),判断的理由是_____________________。
(4)实验前28.8g样品,实验后测得D装置增重8.8g,则样品中Na2CO3质量分数为_______。
【答案】漏斗中与试剂瓶中的液面差保持不再变化 除去空气中CO2,防止影响测量结果 浓硫酸 必要 因为装置E会吸收空气中的二氧化碳和水蒸气,影响测量结果 73.6%
【解析】
(1)依据B中长颈漏斗和广口瓶中液面变化分析判断;
(2)装置A是为了吸收空气中二氧化碳避免影响碳酸钠含量的测定;装置C是浓硫酸干燥生成的二氧化碳气体;
(3)U形管是吸收二氧化碳气体称重来测定碳酸钠含量的方法,若与空气直接接通,会吸收空气中二氧化碳和水蒸气影响测定结果;
(4)D装置吸收的为二氧化碳质量,结合碳元素守恒计算。
(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,利用压强变化和液面变化分析判断,若漏斗中与试剂瓶中的液面差保持不再变化,证明装置气密性完好;
(2)由于空气中也含有二氧化碳,则装置A可吸收空气中的二氧化碳,防止影响实验结果;生成的二氧化碳中含有水蒸气,则装置C中盛装浓硫酸除去二氧化碳中的水份;
(3)由于空气中含有水蒸气和二氧化碳,则在D装置后应再连接E装置,可以利用碱石灰吸收水蒸气和二氧化碳,避免空气中的水蒸气和二氧化碳被E吸收产生误差;
(4)D装置增重8.80g,则产生的二氧化碳为8.8g,n(CO2)=8.8g÷44g/mol=0.2mol,由碳原子守恒可得n(Na2CO3)=0.2mol,则样品中Na2CO3的质量为0.2mol×106g/mol=21.2g,因此质量分数为21.2g/28.8g×100%=73.6%。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案