题目内容
镁砂(MgO)是一种高温耐火材料.如图是氨法制取高纯镁砂的部分工艺流程:
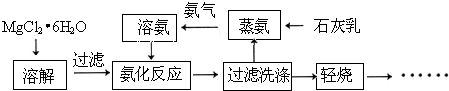
请回答:
(1)MgCl2?6H2O溶于水,溶液呈______(填“酸性”、“中性”、或“碱性”).
(2)蒸氨是将石灰乳通入氯化铵溶液中,并加热,写出该反应的化学方程式:______.
(3)轻烧后的产物为______.
(4)如何检验沉淀已洗涤干净的方法是______.
(5)氨化反应过程中反应的离子方程式为______.
(6)已知向Mg(OH)2沉淀中滴加氯化铵溶液可观察到沉淀溶解,试解释该反应发生的原理(用离子方程式表示和文字说明)______.

请回答:
(1)MgCl2?6H2O溶于水,溶液呈______(填“酸性”、“中性”、或“碱性”).
(2)蒸氨是将石灰乳通入氯化铵溶液中,并加热,写出该反应的化学方程式:______.
(3)轻烧后的产物为______.
(4)如何检验沉淀已洗涤干净的方法是______.
(5)氨化反应过程中反应的离子方程式为______.
(6)已知向Mg(OH)2沉淀中滴加氯化铵溶液可观察到沉淀溶解,试解释该反应发生的原理(用离子方程式表示和文字说明)______.
(1)MgCl2?6H2O溶于水,在溶液中Mg2+发生水Mg2++2H2O?Mg(OH)2+2H+,溶液呈酸性;
故答案为:酸性;
(2)将石灰乳通入氯化铵溶液中并加热产生氨气;
故答案为:Ca(OH)2+2NH4Cl
2NH3↑+CaCl2+2H2O;
(3)过滤洗涤得到Mg(OH)2固体,轻烧发生反应:Mg(OH)2
MgO+2H2O;
故答案为:MgO(或氧化镁);
(4)通过洗涤液中是否存在氯离子检验Mg(OH)2固体是否洗涤干净,方法为,向洗涤后的溶液中滴加硝酸酸化的AgNO3溶液,若无白色沉淀生成,证明已经洗涤干净;
故答案为:向洗涤后的溶液中滴加硝酸酸化的AgNO3溶液,若无白色沉淀生成,证明已经洗涤干净;
(5)溶氨后形成氨水,与MgCl2溶液发生反应生成Mg(OH)2沉淀,方程式为,Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+
,故答案为:Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+;
(6)Mg(OH)2在溶液中存在溶解平衡:Mg(OH)2(s)?Mg2++2OH-,在氯化铵溶液中存在NH4+:NH4++OH-?NH3?H2O?NH3↑+H2O,滴加NH4Cl溶液,振荡使氨气快速逸出,均能使平衡正向移动,导致Mg(OH)2沉淀溶解;
故答案为:Mg(OH)2在溶液中存在溶解平衡:Mg(OH)2(s)?Mg2++2OH-,在氯化铵溶液中存在NH4+:NH4++OH-?NH3?H2O?NH3↑+H2O,滴加NH4Cl溶液,振荡使氨气快速逸出,均能使平衡正向移动,导致Mg(OH)2沉淀溶解;
故答案为:酸性;
(2)将石灰乳通入氯化铵溶液中并加热产生氨气;
故答案为:Ca(OH)2+2NH4Cl
| ||
(3)过滤洗涤得到Mg(OH)2固体,轻烧发生反应:Mg(OH)2
| ||
故答案为:MgO(或氧化镁);
(4)通过洗涤液中是否存在氯离子检验Mg(OH)2固体是否洗涤干净,方法为,向洗涤后的溶液中滴加硝酸酸化的AgNO3溶液,若无白色沉淀生成,证明已经洗涤干净;
故答案为:向洗涤后的溶液中滴加硝酸酸化的AgNO3溶液,若无白色沉淀生成,证明已经洗涤干净;
(5)溶氨后形成氨水,与MgCl2溶液发生反应生成Mg(OH)2沉淀,方程式为,Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+
,故答案为:Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+;
(6)Mg(OH)2在溶液中存在溶解平衡:Mg(OH)2(s)?Mg2++2OH-,在氯化铵溶液中存在NH4+:NH4++OH-?NH3?H2O?NH3↑+H2O,滴加NH4Cl溶液,振荡使氨气快速逸出,均能使平衡正向移动,导致Mg(OH)2沉淀溶解;
故答案为:Mg(OH)2在溶液中存在溶解平衡:Mg(OH)2(s)?Mg2++2OH-,在氯化铵溶液中存在NH4+:NH4++OH-?NH3?H2O?NH3↑+H2O,滴加NH4Cl溶液,振荡使氨气快速逸出,均能使平衡正向移动,导致Mg(OH)2沉淀溶解;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
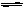 Pb2+(aq)+2I-(aq),下列描述正确的是 ( )
Pb2+(aq)+2I-(aq),下列描述正确的是 ( )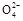 只向PbO2处移动
只向PbO2处移动