题目内容
【题目】如图是电解水制高纯氢的示意图,通过控制开关连接K1或K2,可交替得到H2和O2。下列说法正确的是
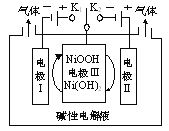
A.制H2时,连接K2
B.连接K1时,电极Ⅰ附近碱性减弱
C.制O2时,电极Ⅲ的反应为:NiOOH+e+H2O=Ni(OH)2+OH-
D.通过控制开关连接K1和K2,可使电极Ⅲ循环使用
【答案】CD
【解析】
该装置为电解池,通过控制开关连接K1或K2电解水,可交替得到H2和O2,在电解池中,阳极发生失电子的氧化反应,阴极发生得电子的还原反应。当开关闭合到K2时,所形成的电解池中,电极II为阳极,电极反应式为:4OH- - 4e- = O2↑+ 2H2O,氧气在电极II生成,此时电极III为阴极,NiOOH中Ni为+3价,Ni(OH)2中Ni为+2价,则NiOOH是反应物,Ni(OH)2是生成物;当开关闭合到K1时,电极III为阳极,NiOOH是生成物,Ni(OH)2是反应物,电极I为阴极,阴极反应式为:2H2O + 2e- = H2↑+2OH-,氢气在电极I生成,据此解答。
该装置为电解池,通过控制开关连接K1或K2电解水,可交替得到H2和O2,在电解池中,阳极发生失电子的氧化反应,阴极发生得电子的还原反应。当开关闭合到K2时,所形成的电解池中,电极II为阳极,电极反应式为:4OH- - 4e- = O2↑ + 2H2O,氧气在电极II生成,此时电极III为阴极,NiOOH中Ni为+3价,Ni(OH)2中Ni为+2价,则NiOOH是反应物,Ni(OH)2是生成物;当开关闭合到K1时,电极III为阳极,NiOOH是生成物,Ni(OH)2是反应物,电极I为阴极,电极反应式为:2H2O + 2e- = H2↑+2OH-,氢气在电极I生成。
A. 由以上分析可知,H2在阴极生成,连接到K1时,电极I为阴极,得到的气体为氢气,A项错误;
B. 连接K1时,电极Ⅰ为阴极,电极反应式为:2H2O + 2e- = H2+2OH-,则电极附近碱性增强,B项错误;
C. 氧气在电极II生成,开关闭合到K2,此时电极III为阴极,电极Ⅲ的反应为:NiOOH+e+H2O=Ni(OH)2+OH-,C项正确;
D. 当开关闭合到K2时,电极III为阴极,电极III反应式为:NiOOH+e+H2O=Ni(OH)2+OH-;当开关闭合到K1时,电极III为阳极,电极III反应式为:Ni(OH)2 - e+OH-=NiOOH+H2O,则通过控制开关连接K1和K2,可使电极Ⅲ循环使用,D项正确;
答案选CD。

 阅读快车系列答案
阅读快车系列答案