题目内容
【题目】下列图示与对应的叙述相符合的是

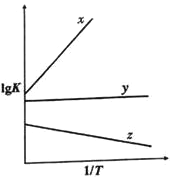
A. 图甲表示对某化学平衡体系改变温度后反应速率随时间的变化
B. 图乙表示反应物断键吸收的能量大于生成物成键放出的能量
C. 图丙表示0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化
D. 图丁表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况
【答案】B
【解析】A、升高温度,正逆反应速率都增大,都大于原来平衡速率,选项A错误;B、反应物断键吸收的能量大于生成物成键放出的能量为吸热反应,该图表示正确,选项B正确;C、图中向20 mL 0.1 mol·L-1硫酸中滴加0.1 mol·L-1NaOH溶液时,溶液酸碱性的变化是:酸性溶液→中性溶液→碱性溶液,但滴定终点消耗氢氧化钠的体积应该为40 mL,选项C错误;D、图丁表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化应逐渐减小,当硫酸过量时导电性逐渐增大,选项D错误。答案选B。

练习册系列答案
相关题目