题目内容
【题目】含硫物质燃烧会产生大量烟气,主要成分是SO2、CO2、N2、O2。某研究性学习小组在实验室利用下列装置制备模拟烟气,并测算模拟烟气通过转化器的脱硫效率。
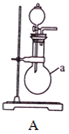
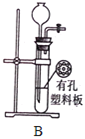
模拟烟气的制备
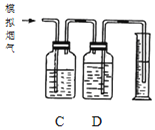
测定烟气中SO2的体积分数 烟气通过转化器脱硫
请回答下列问题:
I. 模拟烟气的制备
(1)用_______装置制SO2,用________装置制CO2(填“A”或“B”)。
(2)将制得的气体与一定量空气充分混合,获得模拟烟气用于后续实验。
Ⅱ. 测定烟气中SO2的体积分数
(3)将部分模拟烟气缓慢通过C、D装置,其中C、D中盛有的药品分别是_______、________。(填序号)
①KMnO4溶液 ②饱和NaHSO3溶液 ③饱和Na2CO3溶液 ④饱和NaHCO3溶液
写出吸收SO2时发生反应的离子方程式_____________________________________________。
(4)若模拟烟气的流速为a mL/min,t1 min后,测得量筒内液体体积为V mL,则SO2的体积分数是_______。
Ⅲ. 测算模拟烟气通过转化器的脱硫效率(已转化的SO2占原有SO2的百分比)
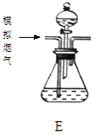
(5)将模拟烟气通过转化器E装置,E装置中盛有FeCl2、FeCl3的混合溶液,常温下,该混合溶液可以催化SO2与O2的反应,以达到更好脱硫的目的。写出催化剂参与反应过程的离子方程式:
①SO2+2H2O+2Fe3+=SO42-+2Fe2++4H+
②_________________________________________________。
(6)若模拟烟气仍以a mL/min的流速通过转化器E装置,t2 min后,向E装置中加入酸化的___________溶液得到白色浑浊液,经一系列操作后,得到m g固体。若实验的气体体积已折算为标准状况,则该转化器的脱硫效率是________________。
【答案】 A B ① ④ 5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+ ![]() 4Fe2++O2+4H+=2H2O+4Fe3+ BaCl2
4Fe2++O2+4H+=2H2O+4Fe3+ BaCl2 ![]()
【解析】I. (1)实验室制备二氧化硫,可以选用亚硫酸钠固体和硫酸反应,亚硫酸钠易溶于水,应该选用A装置制SO2,实验室用碳酸钙与盐酸反应制备二氧化碳,碳酸钙难溶于水,可以选用B装置制CO2,故答案为:A;B;
Ⅱ.(3)二氧化硫具有强的还原性,可以用强氧化性的高锰酸钾吸收;二氧化碳在饱和碳酸钠溶液中的溶解度很小,可以用排饱和碳酸氢钠溶液来侧量其体积,高锰酸钾氧化二氧化硫生成硫酸根离子,反应的离子方程式为5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+,故答案为:①;④;5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+;
(4)若模拟烟气的流速为aml/min,t1分子后测得量筒内液体为VmL,则混合气体二氧化碳、氧气、氮气的体积是Vml,则二氧化硫的体积为t1aml-Vml,所以二氧化硫的体积分数为![]() ×100%=
×100%=![]() %,故答案为:
%,故答案为: ![]() %;
%;
Ⅲ. (5)②SO2+2H2O+2Fe3+═SO42-+2Fe2++4H+ 在反应①中三价铁离子被还原为二价铁离子,要想保持质量、性质不变,得到的二价铁离子应该被氧气氧化为三价铁离子,反应的方程式为:4Fe2++O2+4H+=2H2O+4Fe3+,故答案为:4Fe2++O2+4H+=2H2O+4Fe3+;
(6)若模拟烟气仍以a mL/min的流速通过转化器E装置,t2 min后,向E装置中加入酸化的氯化钡溶液得到硫酸钡沉淀;t2分钟内烟气中含二氧化硫的体积为:V(SO2)=at2×![]() %; 根据上述反应可知各物质之间量的关系为:
%; 根据上述反应可知各物质之间量的关系为:
SO2~SO42-~BaSO4
22400ml233g
V(SO2)′ mg
所以转化的二氧化硫气体的体积为:V(SO2)′=![]() ;所以二氧化硫的转化率=
;所以二氧化硫的转化率=![]() =
=![]() ,故答案为:BaCl2;
,故答案为:BaCl2; ![]() 。
。

 智能训练练测考系列答案
智能训练练测考系列答案