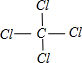题目内容
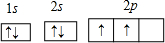
元素A、B、C都是短周期元素,它们的原子序数A<B<C。A元素原子的最外层电子数为次外层电子数的两倍;B元素的原子的次外层电子数是最外层电子数的两倍;B与C可以形成共价化合物BC4。试回答:?(1)三种元素符号:A? ?,B? ?,C? ?。?
(2)气态氢化物化学式依次为? ?、? ?、? ?,其中最不稳定的是? ?,它在空气中燃烧的化学方程式为? ?。?
(3)它们的最高价氧化物对应水化物中酸性最强的是? ?,最弱的是? ?。
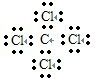
(4)BC4的化学式? ?,电子式? ?。
(1)C Si Cl (2)CH4 SiH4 HCl SiH4?
SiH4+2O2![]() SiO2+2H2O?
SiO2+2H2O?
(3)HClO4 H2SiO3?
 ?
?
解析:要认真剖析题中所给的信息“A元素原子的最外层电子数为次外层电子数的两倍;B元素原子的次外层电子数是最外层电子数的两倍”分析可得出结果。根据上述信息得出2,4排布的碳元素A,2,8,4排布的硅元素B;由于C为短周期元素,且原子序数B<C,又B与C可形成共价化合物BC4,则C元素在BC4中显-1价,故C元素应为氯,依次得出答案。

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目