题目内容
【题目】如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是( )

A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
D.甲池中消耗280mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
【答案】D
【解析】
甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,则甲池为燃料电池,通CH3OH的电极为负极,通O2的电极为正极;乙池,石墨为阳极,Ag为阴极;丙池,左边Pt为阳极,右边Pt为阴极。
A.甲池将化学能转化为电能,乙、丙池将电能转化化学能,A不正确;
B.甲池中通入CH3OH的电极反应式为CH3OH-6e-+8OH- =CO32- +6H2O,B不正确;
C.乙池中,石墨为阳极,电极反应式为2H2O-4e- ==O2↑+4H+,Ag为阴极,电极反应式为2Cu2++4e- ==2Cu,反应一段时间后,向乙池中加入一定量CuO固体能使CuSO4溶液恢复到原浓度,C不正确;
D.依据得失电子守恒,可建立甲池中O2与丙池中Mg(OH)2的关系式为:O2—2Mg(OH)2,n(O2)=![]() =0.0125mol,此时丙池中理论上最多产生Mg(OH)2固体0.0125mol ×2×58g/mol=1.45g,D正确;
=0.0125mol,此时丙池中理论上最多产生Mg(OH)2固体0.0125mol ×2×58g/mol=1.45g,D正确;
故选D。

【题目】下列实验所得结论正确的是
① | ② | ③ | ④ |
|
|
|
|
充分振荡试管,下层溶液红色褪去 | 溶液变红 | 溶液变红 | 充分振荡右侧小试管, 下层溶液红色褪去 |
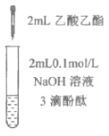
A.①中溶液红色褪去的原因是:CH3COOC2H5+NaOH![]() CH3COONa+C2H5OH
CH3COONa+C2H5OH
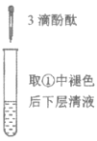
B.②中溶液变红的原因是:CH3COO-+H2O![]() CH3COOH+H+
CH3COOH+H+
C.由实验①、②、③推测,①中红色褪去的原因是乙酸乙酯萃取了酚酞
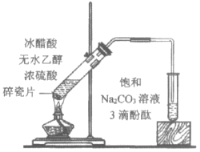
D.④中红色褪去证明右侧小试管中收集到的乙酸乙酯中混有乙酸
【题目】将一定量纯净的氨基甲酸胺(H2NCOONH4)固体,置于特制密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应: H2NCOONH4(s)![]() 2NH3(g)+CO2(g)达到分解平衡,实验测得不同温度及反应时间(t1<t2<t3)的有关表格:
2NH3(g)+CO2(g)达到分解平衡,实验测得不同温度及反应时间(t1<t2<t3)的有关表格:
氨基甲酸铵分解时温度、气体总浓度及反应时间的关系。
温度/℃ 气体总浓度(mol/L) 时间/min | 15 | 25 | 35 |
0 | 0 | 0 | 0 |
t1 | 0.9×10-3 | 2.7×10-3 | 8.1×10-3 |
t2 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
t3 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
(1)在25℃,0-t1时间内产生氨气的平均速率为___。
(2)根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)![]() H2NCOONH4(s)平衡常数K约为___。
H2NCOONH4(s)平衡常数K约为___。
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:CO2(g)+3H2(g)![]() CH3OH(g)+H2(g) ΔH<0在恒温恒容的密闭容器中,加入1molCO2和3molH2,充分反应达平衡时放出热量akJ,若在原容器中加入2molCO2和6molH2,在相同温度下反应达平衡时放热bkJ,则a和b满足的关系___。
CH3OH(g)+H2(g) ΔH<0在恒温恒容的密闭容器中,加入1molCO2和3molH2,充分反应达平衡时放出热量akJ,若在原容器中加入2molCO2和6molH2,在相同温度下反应达平衡时放热bkJ,则a和b满足的关系___。