题目内容
【题目】亚硝酸钠常用作食品防腐剂。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸的反应及生成气体产物的成分。
已知:①NO+NO2+2OH-===2NO![]() +H2O
+H2O
②气体液化的温度:NO2:21℃、NO:-152℃
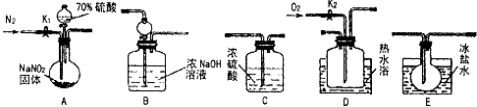
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(按左→右连接):
(2)组装好仪器后,接下来进行的操作是 .
(3)关闭弹簧夹K1,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体中含有NO,依据的现象是___________________。
②装置B的作用是___________________,装置E的作用是____________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为 。如果没有装置C,对实验结论造成的影响是__________________。
【答案】(1)A→C→E →D →B
(2)检查装置的气密性 (1分)
(3)①D中通氧气后,出现红棕色气体 ②吸收NO2和 NO,防止污染空气 冷凝使NO2完全液化
(4)4NO2+O2+4NaOH=4NaNO3+2H2O
水会与NO2反生成应NO,影响后面NO的检验
【解析】
试题分析:(1)此实验的目的探究亚硝酸钠和硫酸反应以及生成气体的产物,A装置是反应装置,B装置是尾气处理装置,C装置是干燥气体,D装置为验证NO气体,E装置冷却NO2,因此连接顺序是A→C→E→D→B;
(2)因为此实验有气体参加,因此实验前,需要检验装置的气密性;
(3)①NO为无色气体,与氧气生成红棕色气体NO2,因此D装置通入氧气后无色变为红棕色,说明NO的存在;②氮的氧化物对环境都是有污染的,必须尾气处理,因此B装置的作用:尾气处理,防止污染空气;NO2的液化温度是21℃,因此E装置的作用:冷凝使NO2完全液化;
(4)通入过量O2,NO全部转化成NO2,因此有分液4NO2+O2+4NaOH=4NaNO3+2H2O,如果没有装置C,水会与NO2反应生成NO,影响后面NO的检查。