题目内容
在0℃和101KPa下,2.00gHe、3.01×1022个N2、1.60gO2混合,该混合气体的体积是( )
| A.13.44L | B.7.84L | C.10.08L | D.无法计算 |
n(He)=
=0.5mol,n(O2)=
=0.05mol,n(N2)=
=0.05mol,则混合气体的总物质的量为:0.5mol+0.05mol+0.05mol=0.6mol,该混合气体的体积V=n?Vm=0.6mol×22.4L/mol=13.44L,
故选:A.
| 2.00g |
| 4g/mol |
| 1.60g |
| 32g/mol |
| 3.01×1022 |
| 6.02×1023mol-1 |
故选:A.

练习册系列答案
相关题目
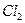 与足量水反应转移电子数约为
与足量水反应转移电子数约为 个
个 个
个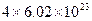 个
个