题目内容
在一定温度下,容器中某一反应有M、N的物质的量随反应时间变化的曲线如下图所示。据此,回答下列有关问题: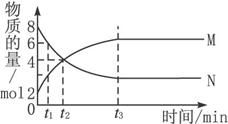
(1)该反应的化学方程式为_______________。
(2)t1时,M与N物质的量浓度的关系为_________。
(3)t2时,v(正)v(逆)_________(填“>”“=”或“<”)。
(4)t3时,图象所代表的意义_________。
解析:(1)从0—t2 (min),变化的M、N物质的量分别为Δn(N)=8 mol-4 mol=4 mol, Δn
(M)=4 mol-2 mol=2 mol,故化学方程式为2N![]() M。
M。
(2)在t1(min)时,n(N)=6 mol,n(M)=3 mol,由于在同一容器中,所以c(N)=2c(M)。
(3)在t2(min)时,从曲线的变化趋势来看,平衡向正反应方向移动,故v(正)>v(逆)。
(4) t3时,由图示可知,M、N的物质的量不随时间而发生变化,说明已达平衡。
答案:(1)2N![]() M (2)c(N)=2c(M) (3)> (4)反应已达平衡状态
M (2)c(N)=2c(M) (3)> (4)反应已达平衡状态

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
在一个固定容积的密闭容器中,充入等物质的量的X和Y,发生如下反应:X(g)+Y(g)?2Z(g),(正反应放热反应);下列说法正确的是( )
| A、当反应达到平衡后,若升高温度,容积内压强不变 | B、当反应达到平衡后,充入Z气体,达到新平衡时,X的体积分数不变,但X的浓度升高 | C、在一定温度下,容器中气体压强增大,但平衡不移动 | D、若向容器内通入少量X,压强增大,但平衡不移动 |
在一定温度下,容器中加入CO和H2O(g)各1mol,发生反应:CO+H2O CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件和CO的起始量不变,一开始就加入4mol H2O(g),则达到平衡时生成的CO2可能是
CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件和CO的起始量不变,一开始就加入4mol H2O(g),则达到平衡时生成的CO2可能是
| A.0.6mol | B.0.95mol | C.1mol | D.1.5mol |
 CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件和CO的起始量不变,一开始就加入4mol H2O(g),则达到平衡时生成的CO2可能是
CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件和CO的起始量不变,一开始就加入4mol H2O(g),则达到平衡时生成的CO2可能是