��Ŀ����
����Ŀ������ȫ����������������Ϊ��Ч�������������ػ�����ȡ��ʩ���ƴ����������о�����Ч���ƿ����е������̼���������Ⱦ����һ����Ҫ����Ĺ�����
��������������о�
��1��һ�������£���2mol NO��2mol O2���ں����ܱ������з�����Ӧ��2NO(g)+O2(g) ![]() 2NO2(g)������״̬��˵���÷�Ӧ�ﵽ��ѧƽ�������_______��
2NO2(g)������״̬��˵���÷�Ӧ�ﵽ��ѧƽ�������_______��
A�����������ܶȱ��ֲ���
B��NO��ת���ʱ��ֲ���
C��NO��O2�����ʵ���֮�ȱ��ֲ���
D��O2���������ʺ�NO2�������������
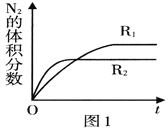
��2����֪��Ӧ. 2NO(g) ![]() N2(g)+O2(g) ��H<O���ڲ�ͬ����ʱN2�����������ʱ��(t)�ı仯��ͼ1��ʾ������ͼ������ж�����R1��R2��Ӧ�����з�Ӧ�����в�ͬ����______ (����ĸ���)��
N2(g)+O2(g) ��H<O���ڲ�ͬ����ʱN2�����������ʱ��(t)�ı仯��ͼ1��ʾ������ͼ������ж�����R1��R2��Ӧ�����з�Ӧ�����в�ͬ����______ (����ĸ���)��
A��ѹǿ B���¶� C������
����ͼ2�е������仯���ݣ����㷴Ӧ2NO(g) ![]() N2(g)+O2(g)����H=__________
N2(g)+O2(g)����H=__________

����̼�������о�
��3��CO��H2��һ�������¿��Ժϳɼ״���CO(g)+2H2(g) ![]() CH3OH(g) ��H<O ���������Ϊ1L�ĺ����ܱ�������ͼ3������ͨ��1mol CO��2mol H2���ⶨ��ͬʱ�䡢��ͬ�¶�(T)��������CO�����ʵ��������±���
CH3OH(g) ��H<O ���������Ϊ1L�ĺ����ܱ�������ͼ3������ͨ��1mol CO��2mol H2���ⶨ��ͬʱ�䡢��ͬ�¶�(T)��������CO�����ʵ��������±���

��ش���
��T1_____ T2������>������<������=������������____________________����֪T2��ʱ����20minʱ������ѹǿ���ٸı䣬��ʱH2��ת����Ϊ_________�����¶��µĻ�ѧƽ�ⳣ��Ϊ________ ��
������1mol CO��2mol H2ͨ��ԭ���Ϊ1L�ĺ�ѹ�ܱ�������ͼ3�����У���T2���´ﵽƽ�⣬��ʱ��Ӧ��ƽ�ⳣ��Ϊ_________;������������ͨ��l mol CH3OH(g)�����´ﵽƽ���CH3OH(g)����ϵ�еİٷֺ���_________(���������������С������������)��
��4��һ��������Ҳ����NaOH��Һ��CO��Ӧ���ɼ����ƣ���һ����Ӧ���ɼ���������CO��Ⱦ�������½�a mol��COͨ��2 L bmol/L NaOH ��Һ�У�ǡ����ȫ��Ӧ���ɼ����ƺͺ���������Ļ����Һ(������Һ�������)�������Һ��c(Na+)=c(HCOO-)����û����Һ�м���ĵ���ƽ�ⳣ�� Ka=____________ (�ú�a��b�Ĵ���ʽ��ʾ)��
���𰸡� BC B ��183kJ.mol-1 �� �¶�Խ�ߣ���Ӧ����Խ�졣������������ͬʱ��T2ʱ�ķ�Ӧ���ʱ�T1�ķ�Ӧ���ʿ� 50%��0.5 1 1 ���� ��2b��10��7��/��a��2b��
����������.(1)A����Ӧ����������Ϊ���壬�����������䣬���������ܶ�ʼ�ձ��ֲ��䣬��A����B��NO��ת���ʱ��ֲ��䣬˵�����淴Ӧ������ͬ��B��ȷ��C��NO��O2��Ͷ�ϱȲ����ڼ�����֮�ȣ�NO��O2�����ʵ���֮�ȱ��ֲ��䣬˵�������ʵ���Ũ�ȱ��ֲ��䣬��C��ȷ��D��O2���������ʺ�NO2�������������ʱ�����淴Ӧ���ʲ����ȣ���D����ѡBC��(2)A��R2��Ӧѹǿ�ߣ���ѹ��ƽ�������ƶ���N2���������Ӧ��Щ����A����B��R2��Ӧ���¶ȸߣ����ȷ�Ӧ�����º�ƽ�������ƶ���N2���������ӦСЩ����B��ȷ��C��������ƽ��û��Ӱ�죬��C����ѡB������ͼ2�е������仯���ݣ����㷴Ӧ2NO(g) ![]() N2(g)+O2(g) �Ħ�H=��������������kJ��mol-1 ����������kJ��mol-1 ��������kJ��mol-1���� -183kJ��mol-1
N2(g)+O2(g) �Ħ�H=��������������kJ��mol-1 ����������kJ��mol-1 ��������kJ��mol-1���� -183kJ��mol-1
��.��������T1��T2���¶�Խ�ߣ���Ӧ����Խ�졣������������ͬʱ��T2ʱ�ķ�Ӧ���ʱ�T1ʱ�ķ�Ӧ���ʿ죻T2��ʱ����20minʱ������ѹǿ���ٸı䣬
CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
nʼ/mol 1 2 0
n��/mol 0.5 1 0.5
nƽ/mol 0.5 1 0.5
cƽ/mol/L 0.5 1 0.5
H2��ת����Ϊ=1mol/2mol��100%=50%,���¶��µĻ�ѧƽ�ⳣ��Ϊ=![]() �����¶Ȳ��䣬ƽ�ⳣ�����䣬��Ϊ1��������������ͨ��1molCH3OH(g)�����´ﵽƽ���CH3OH(g)����ϵ�еİٷֺ������䣬�൱����������Чƽ�⡣
�����¶Ȳ��䣬ƽ�ⳣ�����䣬��Ϊ1��������������ͨ��1molCH3OH(g)�����´ﵽƽ���CH3OH(g)����ϵ�еİٷֺ������䣬�൱����������Чƽ�⡣
(4) �������غ�c(HCOOH)+c��HCOO�D ��= ![]() ��c(Na+)=c(HCOO-)=bmol/L��c(HCOOH)=
��c(Na+)=c(HCOO-)=bmol/L��c(HCOOH)= ![]() ���ɵ���غ�c(H�� )=10-7mol/L,K=
���ɵ���غ�c(H�� )=10-7mol/L,K= ![]() ��10-7��
��10-7��![]()

 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д� Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д�