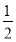题目内容
某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
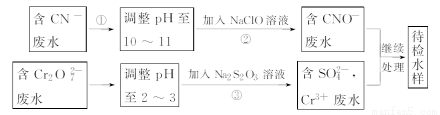
回答下列问题:
(1)上述处理废水流程中主要采用的方法是_____________。
(2)流程②中,反应后无气体放出,该反应的离子方程式为_______。
(3)含Cr3+废水需进一步处理,请你设计一个处理方案:_______。
(4)反应③中,每消耗0.4 mol Cr2O72-转移2.4 mol e-,该反应离子方程式为________。
(1)氧化—还原法
(2)CN-+ClO-=CNO-+Cl- (3)调节废水pH,使其转化成Cr(OH)3沉淀除去(其他合理答案也可)
(4)3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O
【解析】(2)由②中反应后无气体放出,可知其产物为Cl-和CNO-,根据电子守恒配平即可。(4)由消耗0.4 mol Cr2O72-转移2.4 mol e-,可知反应后铬转化为+3价,据此,再根据电子守恒写出离子方程式。

Q、R、T、X、Y、Z是六种原子序数依次增大的前四周期常见元素,其相关信息如下表:
元素 | 相关信息 |
Q | Q的单质是实验室常用的惰性电极材料 |
R | R原子基态时2p原子轨道上有3个未成对电子 |
T | 负二价的元素T的氢化物在通常状况下是一种液体,且其中T的质量分数为88.9% |
X | X是第三周期电负性最大的元素 |
Y | 元素Y位于周期表的第10列 |
Z | Z存在质量数为65,中子数为36的核素 |
(1)Z元素的原子基态时的电子排布式是________。
(2)下列叙述正确的是________(填字母序号)。
a.Q的气态氢化物比R的气态氢化物稳定
b.Q的含氧酸一定比R的含氧酸酸性强
c.R的气态氢化物的熔点在同族元素的氢化物中最低
d.R的第一电离能、电负性都比Q的大
(3)Q和T可形成两种常见化合物,分别表示为QT和QT2。QT分子中σ键和π键的个数比为________;QT2分子中,Q原子采取________杂化。
(4)笑气(R2T)是一种麻醉剂,有关理论认为R2T与QT2分子具有相似的结构。故R2T的空间构型是________,其为________(填“极性”或“非极性”)分子。
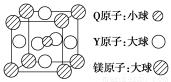
(5)含有Q、Y和镁三种元素的某种晶体具有超导性,其结构如图所示。则该晶体的化学式为________;晶体中每个镁原子周围距离相等且最近的Y原子有______个。