题目内容
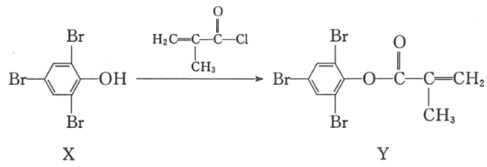
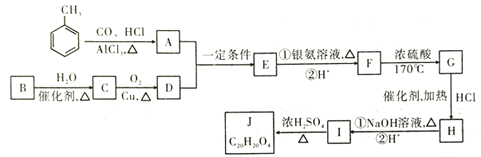
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如图所示:

已知:①RCH2Br![]() R-HC=CH-R’
R-HC=CH-R’
②R-HC=CH-R’![]()
③R-HC=CH-R’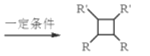
(1)A属于芳香烃,其名称是________________。
(2)B的结构简式是______________________。
(3)由C生成D的化学方程式是__________________。
(4)与![]() 互为同分异构体且符合下列条件的有机物有_________种(不含立体异构)。
互为同分异构体且符合下列条件的有机物有_________种(不含立体异构)。
①苯环上只有两个取代基
②与![]() 含有相同的官能团
含有相同的官能团
③酸性条件下的水解产物能使FeCl3溶液显紫色。
写出其中核磁共振氢谱为五组峰的结构简式:_________(写一种即可)
(5)试剂b是_______________。
(6)下列说法正确的是________(填字母序号)。
a.G存在顺反异构体
b.由G生成H的反应是加成反应
c.1 mol G最多可以与1 mol H2发生加成反应
d.1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 mol NaOH
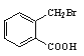
(7)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成![]() ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):_____。
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):_____。
【答案】邻二甲苯 ![]()
 +CH3OH
+CH3OH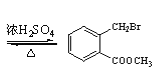 +H2O 15种
+H2O 15种 ![]() NaOH醇溶液 bd
NaOH醇溶液 bd 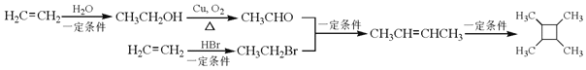
【解析】
由A的分子式、C的结构简式,可知A为![]() ,结合B的分子式与C的结构,可知B为
,结合B的分子式与C的结构,可知B为![]() ,B与液溴在光照条件下反应得到C;由D的分子式、D与HCHO反应所得产物的结构简式,结合已知①,可推知D为
,B与液溴在光照条件下反应得到C;由D的分子式、D与HCHO反应所得产物的结构简式,结合已知①,可推知D为![]() ,则C与甲醇发生酯化反应生成D,故试剂a为CH3OH;D与HCHO反应所得产物发生酯的碱性水解、酸化得到E为
,则C与甲醇发生酯化反应生成D,故试剂a为CH3OH;D与HCHO反应所得产物发生酯的碱性水解、酸化得到E为![]() ;由H的结构、F的分子式,结合已知②可知F为
;由H的结构、F的分子式,结合已知②可知F为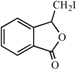 ,对比F、G分子式,可知F发生消去反应生成G为
,对比F、G分子式,可知F发生消去反应生成G为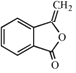 ,试剂b为NaOH醇溶液,G发生已知③中加成反应得到H;
,试剂b为NaOH醇溶液,G发生已知③中加成反应得到H;
(7)由已知③,![]() 可由CH3CH=CHCH3反应得到,由已知①,CH3CH=CHCH3可由CH3CHO和CH3CH2Br生成。乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH发生催化氧化得到CH3CHO;乙烯与HBr发生加成反应得到溴乙烷。
可由CH3CH=CHCH3反应得到,由已知①,CH3CH=CHCH3可由CH3CHO和CH3CH2Br生成。乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH发生催化氧化得到CH3CHO;乙烯与HBr发生加成反应得到溴乙烷。
(1)A是![]() ,其名称是:邻二甲苯;
,其名称是:邻二甲苯;
(2)由分析可知,B的结构简式为:![]() ;
;
(3)由C生成D的化学方程式是: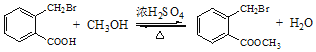 ;
;
(4)与 ![]() 互为同分异构体且符合下列条件的有机物:①苯环上只有两个取代基,②与
互为同分异构体且符合下列条件的有机物:①苯环上只有两个取代基,②与 ![]() 含有相同的官能团,说明含有碳碳双键与酯基,③酸性条件下的水解产物能使FeCl3溶液显紫色,说明含有羧酸与酚形成的酯基,2个取代基为-OOCH、-CH=CHCH3,或者为-OOCH、-CH2CH=CH2,或者为-OOCH、-CH(CH3)=CH2,或者为-OOCCH3、-CH=CH2,或者为-OOCCH=CH2、-CH3,均有邻、间、对3种位置结构,故符合条件的同分异构体共有3×5=15种,其中核磁共振氢谱为五组峰的结构简式:
含有相同的官能团,说明含有碳碳双键与酯基,③酸性条件下的水解产物能使FeCl3溶液显紫色,说明含有羧酸与酚形成的酯基,2个取代基为-OOCH、-CH=CHCH3,或者为-OOCH、-CH2CH=CH2,或者为-OOCH、-CH(CH3)=CH2,或者为-OOCCH3、-CH=CH2,或者为-OOCCH=CH2、-CH3,均有邻、间、对3种位置结构,故符合条件的同分异构体共有3×5=15种,其中核磁共振氢谱为五组峰的结构简式:![]() ;
;
(5)试剂b是 NaOH醇溶液;
(6)a.G为 ,不存在顺反异构体,故a错误;
,不存在顺反异构体,故a错误;
b.G含有碳碳双键,由已知③可知,由G生成H的反应是加成反应,故b正确;
c.G中苯环与碳碳双键能与氢气发生加成反应,1 mol G最多可以与4 mol H2发生加成反应,故c错误;
d.F为 ,含有酯基和I原子,均可与NaOH溶液反应,H含有2个酯基,可与NaOH溶液反应,则1mol F或1mol H与足量NaOH溶液反应,均消耗2molNaOH,故d正确;
,含有酯基和I原子,均可与NaOH溶液反应,H含有2个酯基,可与NaOH溶液反应,则1mol F或1mol H与足量NaOH溶液反应,均消耗2molNaOH,故d正确;
故答案为bd;
(7)由已知③,![]() 由CH3CH=CHCH3反应得到,由已知①,CH3CH=CHCH3可由CH3CHO和CH3CH2Br生成。乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH发生催化氧化得到CH3CHO;乙烯与HBr发生加成反应得到溴乙烷,合成路线流程图为:
由CH3CH=CHCH3反应得到,由已知①,CH3CH=CHCH3可由CH3CHO和CH3CH2Br生成。乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH发生催化氧化得到CH3CHO;乙烯与HBr发生加成反应得到溴乙烷,合成路线流程图为: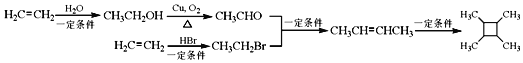 。
。

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案【题目】在金属冶炼产生的废弃物中,常含有砷元素(与磷同主族),由于有毒需检测与处理。
Ⅰ.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
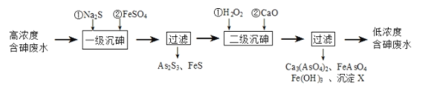
已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq)![]() 2AsS33-(aq);
2AsS33-(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为___;砷酸的第一步电离方程式为__。
(2)“一级沉砷”中FeSO4的作用是___。
(3)“二级沉砷”中H2O2与含砷物质反应的化学方程式为___。沉淀X为___(填化学式)。
Ⅱ.强阴离子交换柱可以吸附以阴离子形态存在的As(V)达到去除As的目的。采用该方法去除水体中的砷时,可选用NaClO将As(Ⅲ)转化为As(V)。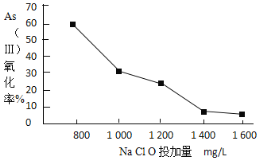
已知:一定条件下,As(V)的存在形式如表所示:
pH | <2 | 2~7 | 7~11 | 11~14 |
存在形式 | H3AsO4 | H2AsO4 | HAsO42 | HAsO42、AsO43 |
(4)pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是___。
Ⅲ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成(即未能检出)。
(5)请写出步骤2的离子方程式____。