题目内容
【题目】用铁和石墨作电极电解酸性废水,可将废水中的PO43-以FePO4(不溶于水)的形式除去,其装置如图所示。
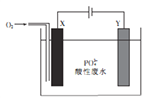
下列说法正确的是
A. 若X、Y电极材料连接反了,则仍可将废水中的PO43-除去
B. X极为石墨,该电极上发生氧化反应
C. 电解过程中Y极周围溶液的pH减小
D. 电解时废水中会发生反应:4Fe2++02-4H++4P043-=4FePO4↓+2H2O
【答案】D
【解析】根据题意分析,X电极材料为铁,Y电极材料为石墨;若X、Y电极材料连接反了,铁就不能失电子变为离子,也就不能生成FePO4,A错误;Y电极材料为石墨,该电极附近发生还原反应,B错误;电解过程中Y极极反应:02+4e-+4H+=2H2O,氢离子浓度减少,溶液的pH变大,C错误;铁在阳极失电子变为Fe2+,通入的氧气把Fe2+氧化为Fe3+,Fe3+与PO43-反应生成FePO4,D正确;正确答案选D。

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目