题目内容
下列离子方程式书写正确的是
| A.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B.明矾溶液中滴加Ba(OH)2溶液至SO42–恰好完全沉淀:Al3++Ba2++ SO42–+3OH–=BaSO4↓+Al(OH)3↓ |
| C.200 mL 2 mol·L–1的FeBr2溶液中通入11.2 L标准状况下的氯气:4 Fe2++6Br–+5Cl2=4Fe3++3Br2+ 10Cl– |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO–+2Fe(OH)3=2FeO42–+3Cl–+H2O+4H+ |
C
试题分析:A、澄清石灰水少量时表现在离子方程式中,OH-应无剩余,而所给离子方程式中Ca2+与OH-的个数比为1:1,化学式中为1:2,所以方程式表达的是石灰水过量,与已知不符,错误;B、明矾的化学式中Al3+与SO42–的个数比为1:2,而该方程式中为1:1,说明SO42–没沉淀完全,错误;C、FeBr2的物质的量为0.4mol,氯气的物质的量为0.5mol,氯气先与Fe2+反应用掉0.2mol,余下的0.3mol与Br–反应,氯气不足,Br–只用掉0.6mol,所以Fe2+、Cl2、Br–的物质的量之比为0.4:0.5:0.6=4:5:6,正确;D、强碱性溶液中,反应后的溶液不会显酸性至大呈中性,错误,答案选C。

练习册系列答案
相关题目
 4OH-+O2↑
4OH-+O2↑
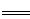 Ca2++H2O+CO2↑
Ca2++H2O+CO2↑