题目内容
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是 ;所含阴离子相同的两种盐的化学式是 。
(2)D的化学式为 ,D溶液显碱性的原因是(用离子方程式表示) 。
(3)E和氨水反应的离子方程式是 。
(4)设计实验检验B中所含的阳离子:
(1)Cu2+、Fe3+ (NH4)2SO4、Al2(SO4)3
(2)Na2CO3 CO32-+H2O?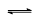 ?HCO3-+OH-
?HCO3-+OH-
(3)Al3++3NH3·H2O==Al(OH)3↓+3NH4+
(4)取少量B于试管中,滴加少量NaOH溶液,在试管口附近放一张湿润的红色石蕊试纸,加热,若试纸变蓝,说明B中阳离子为NH4+
解析试题分析:由①五种盐均溶于水,水溶液均为无色,得出溶液中无Fe3+ 、Cu2+ ,
由②D的焰色反应呈黄色,说明阳离子中一定有Na+ ;
由③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性,说明A是钠盐或钡盐,B、C、E的溶液可能含NH4+ 或Al3+ ,D的溶液是碳酸盐,且只能是Na2CO3;
由④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀,说明A、C的溶液中可能含有Cl―、NO3―;
由⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失,说明E为Al3+ 、结合④C不含Cl―, C为AgNO3;
由⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀,说明A是BaCl2,由⑤得E为Al2(SO4)2,结合③B为(NH4)2SO4,
综上所述:A是BaCl2,B为(NH4)2SO4, C为AgNO3,D是Na2CO3,E为Al2(SO4)2
⑴五种盐中,一定没有的阳离子是溶液呈蓝色的Cu2+、溶液呈黄色的Fe3+ ;所含阴离子相同的两种盐的化学式是(NH4)2SO4、Al2(SO4)3;答案:Cu2+、Fe3+ ;(NH4)2SO4、Al2(SO4)3
⑵D的化学式为Na2CO3,是强碱弱酸盐,在水溶液中发生水解,呈碱性: CO32-+H2O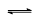 HCO3-+OH-,答案:Na2CO3 CO32-+H2O
HCO3-+OH-,答案:Na2CO3 CO32-+H2O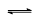 HCO3-+OH-
HCO3-+OH-
⑶E为Al2(SO4)3和氨水反应的离子方程式是Al3++3NH3·H2O==Al(OH)3↓+3NH4+,答案:Al3++3NH3·H2O==Al(OH)3↓+3NH4+
⑷B中所含的阳离子NH4+ ,检验NH4+ 的操作为:取少量B于试管中,滴加少量NaOH溶液,在试管口附近放一张湿润的红色石蕊试纸,加热,若试纸变蓝,说明B中阳离子为NH4+。
考点:常见阳离子的检验;常见阴离子的检验

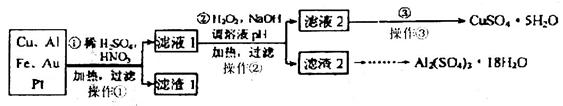
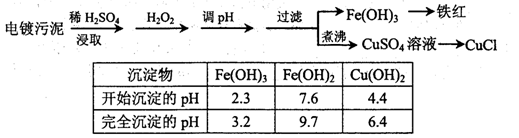
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)反应Ⅰ中发生的氧化还原反应的化学方程式为 。
(2)加入少量NaHCO3的目的是调节pH,使溶液中的________(填“Fe3+”、“Fe2+”或“Al3+”)沉淀。该工艺流程中“搅拌”的作用是______________________。
(3)反应Ⅱ的离子方程式为 ___。在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作____ ____。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为____________________________。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液
从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2等)中回收V2O5的一种生产工艺流程示意图如下,请回答下列问题:
(1)步骤①中废渣的主要成分是 ,③中X试剂为 。
(2)实验室中进行萃取分液操作时,注入萃取剂,充分振荡,将分液漏斗于铁圈上静置,当液体分层后,接下来的操作是 。
(3)②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂)。
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)为提高②中萃取百分率,应采取的措施是 。
2RAn(有机层) + nH2SO4 (水层)为提高②中萃取百分率,应采取的措施是 。
(4)请完成④中的反应离子方程式:
□ClO3- + □VO2+ +□H+ =□VO3+ + □ +□
(5)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH值为 。
(6)该工艺流程中,可以循环利用的物质有 。
 Fe(OH)3+3H+,该反应的平衡常数为 。
Fe(OH)3+3H+,该反应的平衡常数为 。